题目内容
11.下列说法中正确的是( )| A. | 为测定熔融氢氧化钠的导电性,将氢氧化钠固体放在石英坩埚中加热熔化 | |
| B. | 将一定量的Na2O2和NaHCO3的混合物放在一密闭容器中充分加热后,所得固体中一定含有Na2CO3 | |
| C. | 硫酸、纯碱、偏铝酸钠和过氧化钠分别属于酸、碱、盐和氧化物 | |
| D. | 将足量的稀盐酸加到Mg、AlCl3、NaAlO2组成的混合物中,只能发生一种反应 |
分析 A.加热条件下,氢氧化钠和二氧化硅反应;
B.碳酸氢钠加热分解生成二氧化碳和水,二氧化碳先与过氧化钠反应;
C.纯碱属于盐;
D.盐酸和镁、NaAlO2反应.
解答 解:A.加热条件下,氢氧化钠和二氧化硅反应,可使坩埚炸裂,故A错误;
B.碳酸氢钠加热分解生成二氧化碳和水,二氧化碳先与过氧化钠反应生成碳酸钠,故B正确;
C.纯碱为碳酸钠,属于盐,故C错误;
D.盐酸和镁、NaAlO2反应,分别生成氢气、氯化铝、氯化钠,故D错误.
故选B.
点评 本题综合考查元素化合物知识,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
16.下列物质分类正确的是( )
| A. | SO2、SiO2、CO2均为酸性氧化物 | |
| B. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | |
| C. | 烧碱、冰醋酸、四氯化碳、氨气均为电解质 | |
| D. | 福尔马林、水玻璃、氢氟酸、小苏打均为纯净物 |

 .
. .
. .
. .
.
 .
.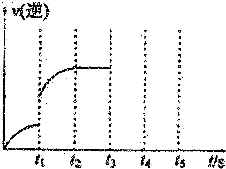 Ⅰ.体积为5L的恒温、恒容密闭容器甲起始投入2molN2、3molH2经过l0s达平衡,测得平衡时NH3的物质的量为0.8mol.
Ⅰ.体积为5L的恒温、恒容密闭容器甲起始投入2molN2、3molH2经过l0s达平衡,测得平衡时NH3的物质的量为0.8mol.