题目内容
13.在Na2S、KOH、CH4、Cl2、Na2O2、H2O2、NH4Cl中,只含有离子键的是Na2S,只含有极性键的是CH4,含有非极性键的是Cl2、Na2O2、H2O2,既含有离子键又有共价键的是KOH、Na2O2、NH4Cl.分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,不同非金属形成极性共价键,同种非金属形成非极性共价键,以此来解答.
解答 解:Na2S只含离子键;
KOH含离子键和O-H极性共价键;
CH4只含C-H极性共价键;
Cl2只含Cl-Cl非极性键;
Na2O2含离子键和O-O非极性共价键;
H2O2含O-H极性共价键和O-O非极性共价键;
NH4Cl中含离子键和N-H极性共价键,
则只含有离子键的是Na2S,只含有极性键的是CH4,含有非极性键的是Cl2、Na2O2、H2O2,既含有离子键又有共价键的是,
故答案为:Na2S;CH4;Cl2、Na2O2、H2O2;KOH、Na2O2、NH4Cl.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.化学与生活息息相关,下列说法错误的是( )
| A. | 用SO2漂白过的草帽辫日久会变色 | |
| B. | 硅胶多孔,常用作食品干燥剂和催化剂的载体 | |
| C. | 黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质 | |
| D. | 氯气处理饮用水,在夏季的杀菌效果比在冬季好 |
1.对 的叙述正确的是( )
的叙述正确的是( )
 的叙述正确的是( )
的叙述正确的是( )| A. | 有两种结构 | B. | 只有一种结构 | C. | 含有非极性键 | D. | 有四种结构 |
8.工业上常利用液晶显示屏生产过程中产生的废玻璃粉末为原料回收金属铈(Ce),金属铈是一种重要的稀土元素,原子序数为58,它有四种同位素,该元素的相对原子质量为140,下列有关说法正确的是( )
| A. | 它是第5周期元素 | |
| B. | 原子核内一定有82个中子 | |
| C. | 铈的四种同位素形成的中性原子,核外电子数相同 | |
| D. | Ce2+中有55个质子 |
18.某有机化合物的结构简式如图所示.有关该化合物的叙述不正确的是( )


| A. | 该有机物的分子式为C11H12O2 | |
| B. | 1 mol该物质最多能与4 mol H2发生加成反应 | |
| C. | 该有机物能与热的新制氢氧化铜悬浊液反应,生成砖红色沉淀 | |
| D. | 该有机物在一定条件下,可以发生取代、氧化、酯化反应 |
2.下列无色溶液中能大量共存的离子组是( )
| A. | Na+、K+、HCO3-、NO3- | B. | K+、Fe3+、NO3-、SCN- | ||
| C. | H+、Cr2O72-、SO42-、K+ | D. | H+、Na+、S2O32-、Cl- |

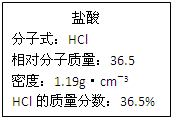 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据