题目内容
工业以CH3OH与NaClO3为原料在酸性条件下制取ClO2,同时产生CO2气体,已知该反应分为两步进行,第一步为2ClO3-+2Cl-+4H+═2ClO2↑+Cl2↑+2H2O.
(1)写出第二步反应的离子方程式 .
(2)工业生产时需在反应物中加少量Cl-,其作用是 .
(3)生产中会发生副反应ClO3-+Cl-+H+-Cl2↑+H2O(未配平),若测得反应后的混合气体中Cl2的体积分数为
,则起始投料时CH3OH与NaClO3的物质的量之比为 .(写出解题过程)
(1)写出第二步反应的离子方程式
(2)工业生产时需在反应物中加少量Cl-,其作用是
(3)生产中会发生副反应ClO3-+Cl-+H+-Cl2↑+H2O(未配平),若测得反应后的混合气体中Cl2的体积分数为
| 3 |
| 73 |
考点:化学方程式的有关计算
专题:计算题,卤族元素
分析:(1)CH3OH与NaClO3为原料在酸性条件下制取ClO2,同时产生CO2气体,则该反应方程式为
CH3OH+6ClO3-+6H+=6ClO2↑+CO2↑+5H2O,将总方程式减去第一步反应方程式即得第二步反应方程式;
(2)氯离子在第一步作反应物、在第二步作生成物;
(3)根据方程式中物理量计算.
CH3OH+6ClO3-+6H+=6ClO2↑+CO2↑+5H2O,将总方程式减去第一步反应方程式即得第二步反应方程式;
(2)氯离子在第一步作反应物、在第二步作生成物;
(3)根据方程式中物理量计算.
解答:
解:(1)由题中给出的反应物和生成物写出总的离子方程式再叠减第一步的离子方程式得出第二步的离子方程式为CH3OH+3Cl2+H2O=6Cl-+CO2+6H+,
故答案为:CH3OH+3Cl2+H2O=6Cl-+CO2+6H+;
(2)通过分析离子方程式得出,Cl-没有参加反应,作为催化剂,故答案为:催化剂;
(3)工业以CH3OH与NaClO3为原料在酸性条件下制取ClO2,同时产生CO2气体,(一般用硫酸酸化)涉及反应的化学方程式为①CH3OH+6NaClO3+3H2SO4→6ClO2+CO2+3Na2SO4+5H2O,生产中会发生副反应②ClO3-+5Cl-+6H+=3Cl2↑+3H2O,生成气体为ClO2、CO2和Cl2,若测得反应后的混合气体中Cl2的体积分数为
,由①可知,如ClO2为60mol,则CO2为10mol,Cl2为3mol,则需要10molCH3OH,(60+1)molNaClO3,则二者体积之比为10:61=1:6.1,
故答案为:1:6.1.
故答案为:CH3OH+3Cl2+H2O=6Cl-+CO2+6H+;
(2)通过分析离子方程式得出,Cl-没有参加反应,作为催化剂,故答案为:催化剂;
(3)工业以CH3OH与NaClO3为原料在酸性条件下制取ClO2,同时产生CO2气体,(一般用硫酸酸化)涉及反应的化学方程式为①CH3OH+6NaClO3+3H2SO4→6ClO2+CO2+3Na2SO4+5H2O,生产中会发生副反应②ClO3-+5Cl-+6H+=3Cl2↑+3H2O,生成气体为ClO2、CO2和Cl2,若测得反应后的混合气体中Cl2的体积分数为
| 3 |
| 73 |
故答案为:1:6.1.
点评:本题考查了物质的量的有关计算,根据总方程式与分步反应方程式的关系书写第二步离子方程式,再结合方程式中各个物理量之间的关系式计算甲醇和氯酸钠的物质的量之比,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 大气臭氧层的分解反应时O3(g)+O(g)═2O2(g)△H,该反应的能量变化如图所示,已知氯原子对O3分解的催化原理为O3(g)+Cl(g)═ClO(g)+O2(g)△H1,ClO(g)+O(g)═Cl(g)+O2(g)△H2.下列判断正确的是( )
大气臭氧层的分解反应时O3(g)+O(g)═2O2(g)△H,该反应的能量变化如图所示,已知氯原子对O3分解的催化原理为O3(g)+Cl(g)═ClO(g)+O2(g)△H1,ClO(g)+O(g)═Cl(g)+O2(g)△H2.下列判断正确的是( )| A、△H=E2-E3 |
| B、E1-E3=△H1+△H2 |
| C、氯原子可使E1减少 |
| D、2O2═O3+O是吸热反应 |
下列说法正确的是( )
| A、在含2mol Si-O键的二氧化硅晶体中,氧原子的数目为4NA |
| B、30g二氧化硅晶体中含有0.5NA个二氧化硅分子 |
| C、金刚石晶体中,碳原子数与C-C键数之比为1:2 |
| D、晶体硅、晶体氖均是由相应原子直接构成的原子晶体 |
下列离子或分子组中能大量共存,且满足相应要求的是( )
| A、K+、AlO2-、Cl-、MnO4- 要求:无色澄清溶液 |
| B、Fe3+、NO3-、I-、HCO3- 要求:逐滴滴加盐酸立即有气体产生 |
| C、Na+、Al3+、Cl-、SO42- 逐滴滴加NaOH先有沉淀产生,后沉淀消失 |
| D、NH4+、Mg2+、SO42-、CH3COOH 要求:滴加NaOH浓溶液立刻又气体产生 |
 在体积为3L的密闭容器中,CO和H2在一定条件下反应生成甲醇:
在体积为3L的密闭容器中,CO和H2在一定条件下反应生成甲醇:


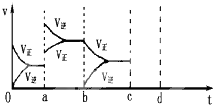 如图表示在密闭容器中反应:CO2(g)+C(s)?2CO(g)△H>0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是
如图表示在密闭容器中反应:CO2(g)+C(s)?2CO(g)△H>0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是