题目内容
下列离子或分子组中能大量共存,且满足相应要求的是( )
| A、K+、AlO2-、Cl-、MnO4- 要求:无色澄清溶液 |
| B、Fe3+、NO3-、I-、HCO3- 要求:逐滴滴加盐酸立即有气体产生 |
| C、Na+、Al3+、Cl-、SO42- 逐滴滴加NaOH先有沉淀产生,后沉淀消失 |
| D、NH4+、Mg2+、SO42-、CH3COOH 要求:滴加NaOH浓溶液立刻又气体产生 |
考点:离子共存问题
专题:离子反应专题
分析:A.无色透明溶液中不存在有色离子,高锰酸根离子为有色离子;
B.铁离子能够与碘离子、碳酸氢根离子发生反应;
C.Na+、Al3+、Cl-、SO42-之间不发生反应,滴加氢氧化钠溶液会生成氢氧化铝沉淀,氢氧化钠过量后沉淀溶解;
D.滴加氢氧化钠溶液后,醋酸优先与氢氧化钠反应,不会生成氨气.
B.铁离子能够与碘离子、碳酸氢根离子发生反应;
C.Na+、Al3+、Cl-、SO42-之间不发生反应,滴加氢氧化钠溶液会生成氢氧化铝沉淀,氢氧化钠过量后沉淀溶解;
D.滴加氢氧化钠溶液后,醋酸优先与氢氧化钠反应,不会生成氨气.
解答:
解:A.无色溶液中不能存在有色的MnO4- 离子,故A错误;
B.Fe3+与I-、HCO3-之间能够发生反应,在溶液中不能大量共存,故B错误;
C.Na+、Al3+、Cl-、SO42-之间不反应,加入氢氧化钠溶液后生成氢氧化铝沉淀,氢氧化钠过量后氢氧化铝沉淀溶解,满足题干要求,故C正确;
D.溶液中加入氢氧化钠浓溶液后,CH3COOH优先与氢氧化钠发生反应,所以不会立刻生成气体,故D错误;
故选C.
B.Fe3+与I-、HCO3-之间能够发生反应,在溶液中不能大量共存,故B错误;
C.Na+、Al3+、Cl-、SO42-之间不反应,加入氢氧化钠溶液后生成氢氧化铝沉淀,氢氧化钠过量后氢氧化铝沉淀溶解,满足题干要求,故C正确;
D.溶液中加入氢氧化钠浓溶液后,CH3COOH优先与氢氧化钠发生反应,所以不会立刻生成气体,故D错误;
故选C.
点评:本题考查离子共存的正误判断,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在等.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
有10g不纯CaCO3样品与足量盐酸作用后生成4.44g CO2,且溶液中残留难溶物质.则对于此样品中是否存在①MgCO3②K2CO3③SiO2杂质的判断正确的是( )
| A、肯定含①③,不含② |
| B、肯定含①③,可能含② |
| C、肯定含②③,不含① |
| D、肯定含②③,可能含① |
在Na2SO4和Al2(SO4)3的混合液中,Al3+和SO42-的物质的量浓度分别为0.2mol/L、0.4mol/L,混合液中Na+的物质的量浓度为( )mol/L.
| A、0.4mol/L |
| B、0.3mol/L |
| C、0.2mol/L |
| D、0.1mol/L |
对于反应3Cl2+6NaOH═5NaCl+NaClO3+3H2O,以下叙述不正确的是( )
| A、NaClO3中Cl的化合价是+5 |
| B、被氧化的Cl原子和被还原的Cl原子的物质的量的比为1:5 |
| C、Cl2既是氧化剂又是还原剂 |
| D、每生成1mol的NaClO3转移6mol的电子 |
在25℃时,物质的浓度相等的NH4Cl、CH3COONH4、NH4HSO4的溶液中,其对应溶液中NH4+的物质的量浓度分别为a、b、c(单位为mol?L-1),下列判断正确的是( )
| A、a=b=c |
| B、a=c>b |
| C、b>a>c |
| D、c>a>b |
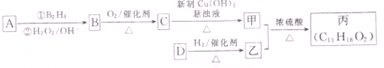
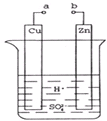 原电池是化学对人类的一项重大贡献.
原电池是化学对人类的一项重大贡献. 