题目内容
16.锌粒和盐酸反应一段时间后,反应速率减慢.此时加热或加入浓盐酸,反应速率明显加快.上述实验中影响化学反应速率的因素有( )①温度 ②固体的表面积 ③反应物的状态 ④溶液的浓度 ⑤催化剂.
| A. | ①④ | B. | ①③ | C. | ②④ | D. | ①②③④⑤ |
分析 影响反应速率的因素有:温度、浓度、催化剂、固体的表面积等,结合外界条件的变化以及反应速率的变化判断..
解答 解:随着反应的进行,溶液浓度减小,反应速率减小,加入浓盐酸,浓度增大,反应速率增大,升高温度,反应速率增大,说明温度对反应速率有影响,
故选A.
点评 本题考查影响化学反应速率的因素,为高频考点,侧重于学生的分析能力的考查,注意把握影响反应速率的条件,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.少量铁粉与100mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,以下方法中可行的是( )
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体 ⑤加NaCl溶液 ⑥滴加几滴硫酸铜溶液
⑦从常温升高到30℃(不考虑盐酸挥发) ⑧改用10mL 0.1mol/L的盐酸.
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体 ⑤加NaCl溶液 ⑥滴加几滴硫酸铜溶液
⑦从常温升高到30℃(不考虑盐酸挥发) ⑧改用10mL 0.1mol/L的盐酸.
| A. | ①⑥⑦ | B. | ③⑤⑧ | C. | ③⑦⑧ | D. | ⑤⑥⑧ |
7.下表为元素周期表的一部分,请回答有关问题:
(1)元素⑤的名称是硅,表中最活泼的金属是K(填写元素符号).
(2)表中能形成两性氢氧化物的元素是Al(填写元素符号),请写出该元素的氢氧化物与⑨的最高价氧化物对应水化物反应的化学方程式Al(OH)3+KOH=KAlO2+2H2O.
(3)元素⑥氢化物的化学式为H2S,其稳定性比H2O弱(填“强”或“弱”)
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | O | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中能形成两性氢氧化物的元素是Al(填写元素符号),请写出该元素的氢氧化物与⑨的最高价氧化物对应水化物反应的化学方程式Al(OH)3+KOH=KAlO2+2H2O.
(3)元素⑥氢化物的化学式为H2S,其稳定性比H2O弱(填“强”或“弱”)
4.已知甲、乙、丙、丁四种物有如下转化关系,其中甲、乙、丁均能发生银镜反应,则甲为( )
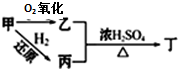

| A. | 甲醇 | B. | 甲醛 | C. | 乙酸 | D. | 乙醛 |
11.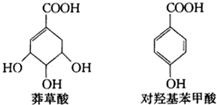 以莽草酸为原料,经多步反应可制取对羟基苯甲酸.莽草酸、对羟基苯甲酸的结构简式如图.下列说法正确的是( )
以莽草酸为原料,经多步反应可制取对羟基苯甲酸.莽草酸、对羟基苯甲酸的结构简式如图.下列说法正确的是( )
 以莽草酸为原料,经多步反应可制取对羟基苯甲酸.莽草酸、对羟基苯甲酸的结构简式如图.下列说法正确的是( )
以莽草酸为原料,经多步反应可制取对羟基苯甲酸.莽草酸、对羟基苯甲酸的结构简式如图.下列说法正确的是( )| A. | 莽草酸、对羟基苯甲酸都属于芳香族化合物 | |
| B. | 1mol莽草酸与NaOH溶液反应,最多消耗4 mol NaOH | |
| C. | 利用FeCl3溶液可鉴别莽草酸和对羟基苯甲酸 | |
| D. | 对羟基苯甲酸较稳定,在空气中不易被氧化 |
1.化学与生活密切相关,下列有关说法不正确的是( )
| A. | 淀粉、蛋白质、脂肪都属于营养物质 | |
| B. | 误食重金属盐,可立即喝牛奶或生蛋清进行解毒 | |
| C. | 棉线和毛线的主要成分都是纤维素 | |
| D. | 新居室内装饰材料中缓慢释放出的甲醛等有机物会污染室内空气 |
8.下列各组指定物质的同分异构体数目相等的是( )
| A. | 苯的二氯代物和苯的一硝基代物 | B. | C3H6Br2和C5H11Br | ||
| C. | 乙烷的二氯代物和丙烷的一氯代物 | D. | 丙烷的一氯代物和戊烷 |
5.下列物质不能使品红溶液褪色的是( )
| A. | SO2 | B. | Cl2 | C. | O3 | D. | CO2 |
6.下列说法正确的是( )
| A. | 化学反应的能量变化都表现为热量的变化 | |
| B. | 任何化学反应都伴有能量的变化 | |
| C. | 反应物的总能量低于生成物的总能量时,发生放热反应 | |
| D. | 反应物的总能量高于生成物的总能量时,发生吸热反应 |