题目内容
20.在100℃时,3.6g CO和H2的混合气体与足量的氧气反应后通入装有足量Na2O2的反应管充分反应,已知CO和H2的质量比为5:1,则反应管增重( )| A. | 5.6 | B. | 1.6 | C. | 3.2 | D. | 3.6 |
分析 CO在氧气中完全燃烧生成CO2,生成的CO2再与Na2O2反应,有关反应为:2CO+O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2,2CO2+2Na2O2=2Na2CO3+O2,总方程式为:2CO+2Na2O2=2Na2CO3,质量增重为CO的质量;H2在氧气中完全燃烧H2O,H2O再与Na2O2反应,有关反应为:2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O,2H2O+2Na2O2=4NaOH+O2,总方程式为:2H2+2Na2O2=4NaOH,质量增重为氢气质量,以此解答.
解答 解:CO在氧气中完全燃烧生成CO2,生成的CO2再与Na2O2反应,有关反应为:2CO+O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2,2CO2+2Na2O2=2Na2CO3+O2,总方程式为:2CO+2Na2O2=2Na2CO3,质量增重为CO的质量;H2在氧气中完全燃烧H2O,H2O再与Na2O2反应,有关反应为:2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O,2H2O+2Na2O2=4NaOH+O2,总方程式为:2H2+2Na2O2=4NaOH,质量增重为氢气质量,综上分析,最终固体增重为CO与氢气的总质量,故3.6gCO和H2的混合气点燃后,再通入足量的Na2O2中,充分反应后,固体增重质量是3.6g,故选D.
点评 本题考查混合物的计算,侧重于学生的分析能力和计算能力的考查,难度中等,注意利用差量法从总反应方程式分析固体质量变化,是解答该题的关键.

练习册系列答案
相关题目
11.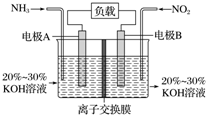 利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是( )
利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是( )
 利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是( )
利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是( )| A. | 电子从右侧电极经过负载后流向左侧电极 | |
| B. | 为使电池持续放电,离子交换膜需选用阴离子交换膜 | |
| C. | 电极A极反应式为2NH3-6e-+6OH-═N2+6H2O | |
| D. | 当有4.48 L NH3 (标准状况)反应时,转移电子为0.6 mol |
8.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程.反应过程的示意图如下:
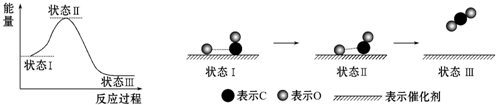
下列说法正确的是( )

下列说法正确的是( )
| A. | CO和O生成CO2是吸热反应 | |
| B. | 在该过程中,CO断键形成C和O | |
| C. | 状态Ⅰ→状态Ⅲ表示CO和O反应生成CO2的过程 | |
| D. | 状态Ⅰ→状态Ⅲ表示CO与O2反应生成CO2的过程 |
15.图是实验室制备氯气并进行一系列相关实验的装置.
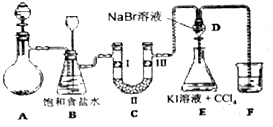
(1)制备氯气选用的药品为:高锰酸钾和浓盐酸,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+8H2O+5Cl2↑.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入D.
(4)设计装置D、E的目的是比较Cl2、Br2、I2的氧化性强弱,当向D中缓慢通入足量氯气时,可以看到无色溶液逐渐变为红棕色,说明Cl2的氧化性大于Br2,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是E中溶液分为两层,下层(CCl4层)为紫红色,该现象不能(填“能”或“不能”)说明Br2的氧化性强于I2.
(5)多余的Cl2用氢氧化钠吸收的离子方程式为Cl2+2OH-=ClO-+H2O.

(1)制备氯气选用的药品为:高锰酸钾和浓盐酸,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+8H2O+5Cl2↑.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入D.
| 选项 | Ⅰ | Ⅱ | Ⅲ |
| A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| B | 干燥的有色布条 | 硅胶 | 湿润的有色布条 |
| C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| D | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(5)多余的Cl2用氢氧化钠吸收的离子方程式为Cl2+2OH-=ClO-+H2O.
12.科学家刚刚发现了某种元素的原子,其质量是a g,12C的原子质量是b g,NA为阿伏加德罗常数的数值,下列说法不正确的是( )
| A. | 该原子的摩尔质量是aNA | |
| B. | Wg该原子的物质的量一定是$\frac{W}{a{N}_{A}}$mol | |
| C. | Wg该原子中含有$\frac{W}{a}$个该原子 | |
| D. | 由已知信息可得:NA=$\frac{12}{b}$ |
9.相对分子质量为M的气态化合物V L(标准状况下),溶于m g水中,得到质量分数为w 的溶液,物质的量浓度为c mol/L,密度为d g/mL,则下列说法不正确的是( )
| A. | 相对分子质量 M=$\frac{22.4mw}{[(1-w)V]}$ | B. | 物质的量浓度 c=$\frac{1000dV}{(MV+22.4m)}$ | ||
| C. | 溶质的质量分数 w=$\frac{MV}{22.4m}$ | D. | 溶液密度 d=$\frac{cM}{1000w}$ |