��Ŀ����
�ס��ҡ���Ϊ�������ʣ��ҡ�����Ԫ�������ڱ���λ��ͬһ���壮X��A��B��C��D��E��F��G��Ϊ�����Ļ��������A��X��Ħ��������ͬ��A��G����ɫ��ӦΪ��ɫ����һ�������£��������ת����ϵ��ͼ����ش�
��1��д��ѧʽ���� ��E ��
��2���õ���ʽ��ʾX���γɹ��� ��
��3��д��A��H2O��Ӧ�Ļ�ѧ��Ӧ����ʽ�� ��
��4��д��B��G��Һ��Ӧ����F�����ӷ���ʽ�� ��
��5������ͼ�ķ�Ӧ�У�������������ԭ��Ӧ���ǣ�����ţ� ��

��1��д��ѧʽ����
��2���õ���ʽ��ʾX���γɹ���
��3��д��A��H2O��Ӧ�Ļ�ѧ��Ӧ����ʽ��
��4��д��B��G��Һ��Ӧ����F�����ӷ���ʽ��
��5������ͼ�ķ�Ӧ�У�������������ԭ��Ӧ���ǣ�����ţ�

���㣺������ƶ�
ר�⣺
�������ס��ҡ���Ϊ���ʣ�A��G����ɫ��ӦΪ��ɫ˵������NaԪ�أ�A�ܺͶ�����̼��Ӧ���ɵ��ʱ�����AΪNa2O2������O2��F��Na2CO3�������Na���������ƺ�ˮ��Ӧ�����������ƺ���������B��NaOH���������ƺ�G��Ӧ����̼���ƣ���G�к�����Ԫ�أ���G��NaHCO3���ҡ�����Ԫ�������ڱ���λ��ͬһ���壬����ΪS��X��Na2S��D��SO2��EΪSO3����������������Ʒ���������ԭ��Ӧ���������ƣ�����C��Na2SO4��
���
�⣺�ס��ҡ���Ϊ���ʣ�A��G����ɫ��ӦΪ��ɫ˵������NaԪ�أ�A�ܺͶ�����̼��Ӧ���ɵ��ʱ�����AΪNa2O2������O2��F��Na2CO3�������Na���������ƺ�ˮ��Ӧ�����������ƺ���������B��NaOH���������ƺ�G��Ӧ����̼���ƣ���G�к�����Ԫ�أ���G��NaHCO3���ҡ�����Ԫ�������ڱ���λ��ͬһ���壬����ΪS��X��Na2S��D��SO2��EΪSO3����������������Ʒ���������ԭ��Ӧ���������ƣ�����C��Na2SO4��
��1��������������֪����ΪO2��EΪSO3���ʴ�Ϊ��O2��SO3��
��2��X��Na2S���õ���ʽ��ʾNa2S���γɹ���Ϊ�� ��
��
�ʴ�Ϊ�� ��
��
��3��A��Na2O2����H2O��Ӧ�Ļ�ѧ��Ӧ����ʽ��2Na2O2+2H2O�T4NaOH+O2����
�ʴ�Ϊ��2Na2O2+2H2O�T4NaOH+O2����
��4��B��G���������ƺ�̼��������Һ�ķ�Ӧ����Ӧ�����ӷ���ʽΪ��HCO3-+H+=CO32-+H2O��
�ʴ�Ϊ��HCO3-+H+=CO32-+H2O��
��5����ͼ��-��ķ�Ӧ�У��١��ڡ��۶����е��ʲμӵĻ��Ϸ�Ӧ��Ϊ������ԭ��Ӧ���ܢݢޢ�����Ԫ�صĻ��ϼ۱仯��������ԭ��Ӧ������Ǹ��ֽⷴӦ�����Բ�����������ԭ��Ӧ���Ǣ�ᣬ�ʴ�Ϊ����ᣮ
��1��������������֪����ΪO2��EΪSO3���ʴ�Ϊ��O2��SO3��
��2��X��Na2S���õ���ʽ��ʾNa2S���γɹ���Ϊ��
 ��
���ʴ�Ϊ��
 ��
����3��A��Na2O2����H2O��Ӧ�Ļ�ѧ��Ӧ����ʽ��2Na2O2+2H2O�T4NaOH+O2����
�ʴ�Ϊ��2Na2O2+2H2O�T4NaOH+O2����
��4��B��G���������ƺ�̼��������Һ�ķ�Ӧ����Ӧ�����ӷ���ʽΪ��HCO3-+H+=CO32-+H2O��
�ʴ�Ϊ��HCO3-+H+=CO32-+H2O��
��5����ͼ��-��ķ�Ӧ�У��١��ڡ��۶����е��ʲμӵĻ��Ϸ�Ӧ��Ϊ������ԭ��Ӧ���ܢݢޢ�����Ԫ�صĻ��ϼ۱仯��������ԭ��Ӧ������Ǹ��ֽⷴӦ�����Բ�����������ԭ��Ӧ���Ǣ�ᣬ�ʴ�Ϊ����ᣮ
���������⿼��������ƶϣ��漰Na��SԪ�ؼ��仯����������ת����������ɫ��Ӧ�Ƴ���ΪNa��AΪNa2O2Ϊ����ͻ�ƿڣ���Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ����С״Ԫ��������������ϵ�д�
����С״Ԫ��������������ϵ�д�
�����Ŀ
��һ������������Ϊ�ϳɵĵ����ǣ�������
A�� |
| B��H2N��CH2��5COOH |
| C��HO��CH2��5COOH��HO��CH2��5NH2 |
| D��HOOC��CH2��4COOH��H2N��CH2��5NH2 |
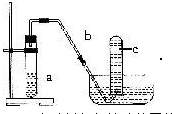
 ʵ������ȡ��ϩ��װ������ͼ��ʾ����ش�
ʵ������ȡ��ϩ��װ������ͼ��ʾ����ش�
 ��ͼ��ʾ��ˮ�����Թ�����һö���������������۲죺
��ͼ��ʾ��ˮ�����Թ�����һö���������������۲죺