题目内容
有一种称为“摇头丸”的毒品己从国外流入我国某些省市,我司法机关坚决予以了查缉和打击.已知这种毒品中氮元素的质量分数为10.37%,它的结构简式可能是( )
A、 |
B、 |
C、 |
D、 |
考点:元素质量分数的计算
专题:有机物分子组成通式的应用规律
分析:根据各选项中的结构简式书写出其分子式,再根据N元素质量分数=
×100%计算各分子式中N元素的质量分数,据此进行判断.
| N原子相对原子质量×N原子数目 |
| 相对分子质量 |
解答:
解:A. 的分子式为C6H7N,N元素质量分数=
的分子式为C6H7N,N元素质量分数=
×100%=15.05%,故A不符合;
B. 的分子式为C9H13N,N元素质量分数=
的分子式为C9H13N,N元素质量分数=
×100%=10.37%,故B符合;
C. 的分子式为C6H5NO2,N元素质量分数=
的分子式为C6H5NO2,N元素质量分数=
×100%=10.53%,故C不符合;
D. 的分子式为C10H15NO,N元素质量分数=
的分子式为C10H15NO,N元素质量分数=
×100%=8.48%,故D不符合;
故选B.
 的分子式为C6H7N,N元素质量分数=
的分子式为C6H7N,N元素质量分数=| 14 |
| 12×6+7+14 |
B.
 的分子式为C9H13N,N元素质量分数=
的分子式为C9H13N,N元素质量分数=| 14 |
| 12×9+13+14 |
C.
 的分子式为C6H5NO2,N元素质量分数=
的分子式为C6H5NO2,N元素质量分数=| 14 |
| 12×6+5+14+16×2 |
D.
 的分子式为C10H15NO,N元素质量分数=
的分子式为C10H15NO,N元素质量分数=| 14 |
| 12×10+15+14+16 |
故选B.
点评:本题以摇头丸结构简式的确定为载体,考查根据化学式计算元素质量分数,比较基础,注意验证法的利用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
光照AgNO3,收集到aL气体(标准状况),反应中转移的电子数为b mol,则标准状况的气体摩尔体积Vm(L/mol)可以表示为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
质量相同的两种气体A、B,在同温同压下,A的密度小于B,下列说法错误的是( )
| A、A的体积比B大 |
| B、A的摩尔质量比B大 |
| C、A的分子数比B多 |
| D、A的物质的量比B大 |
对1mol/L的Na2SO4溶液的叙述中正确的是( )
| A、溶液中含有1 mol Na2SO4 |
| B、1 L溶液中含有142 g Na2SO4 |
| C、1 mol Na2SO4溶于1 L水 |
| D、从1 L该溶液中取出500 mL以后,剩余溶液的浓度为0.5 mol/L |
下列判断正确的是( )
| A、1L H2SO4溶液中含有98g H2SO4,则该溶液的物质的量浓度为98g/L |
| B、1LH2O中溶解了0.5molNaCl,则该溶液的物质的量浓度为0.5mol/L |
| C、从1L 1mol/L 蔗糖溶液中取出100mL溶液,其物质的量浓度仍为1mol/L |
| D、0.5mol/L 的NaOH溶液中,含有0.5mol Na+ |
据图判断下列说法不正确的是( )
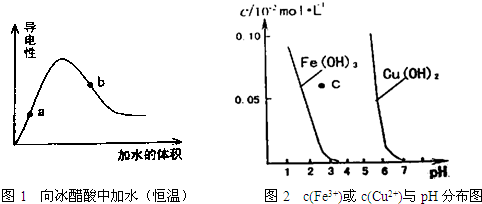

| A、图1中醋酸电离平衡常数:a点的比b点的小 |
| B、图1中醋酸溶液的pH:a点的比b点的大 |
| C、图2中c点对应的溶液为Fe(OH)3的不饱和溶液 |
| D、由图2可知,欲除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调PH约为4左右 |
常温下,下列有关叙述正确的是( )
| A、pH=6的酸性溶液中,可能存在NH3?H2O分子 |
| B、由水电离出来的C(H+)=10-12mol/L的溶液中,Al3+不可能大量存在 |
C、酸性溶液中,可能大量存在Fe3+、SO42-、Na+, |
| D、常温下,C(H+)=0.1mol?L?1的溶液中可能大量存在NO3-、Na+、I-、K+ |
