题目内容
下列说法正确的是( )
| A、200mL1mol/LAl2(SO4)3溶液中,Al3+和SO42-离子总数小于6.02×1023 |
| B、标准状况下,22.4LCl2和HCl的混合气体中含分子总数为2×6.02×1023 |
| C、0.1mol35Cl原子中含中子数为3.5×6.02×1023 |
| D、30g甲醛(CH2O)中共含有电子数为4×6.02×1023 |
考点:阿伏加德罗常数,物质的量的相关计算
专题:计算题,阿伏加德罗常数和阿伏加德罗定律
分析:A.硫酸铝溶液中铝离子部分水解,溶液中铝离子数目减少;
B.标准状况下,22.4L氯气和氯化氢的混合气体的物质的量为1mol;
C.中子数=质量数-质子数,35Cl原子中含有18个中子,0.1mol该氯原子中含有1.8mol中子;
D.甲醛分子中含有16个电子,30g甲醛的物质的量为1mol,含有16mol电子.
B.标准状况下,22.4L氯气和氯化氢的混合气体的物质的量为1mol;
C.中子数=质量数-质子数,35Cl原子中含有18个中子,0.1mol该氯原子中含有1.8mol中子;
D.甲醛分子中含有16个电子,30g甲醛的物质的量为1mol,含有16mol电子.
解答:
解:A.200mL 1mol/L的硫酸铝溶液中含有溶质硫酸铝0.2mol,含有0.6mol硫酸根离子,由于铝离子部分水解,溶液中铝离子的物质的量小于0.4mol,所以溶液中铝离子和硫酸根离子的物质的量之和小于1mol,Al3+和SO42-离子总数小于6.02×1023,故A正确;
B.准状况下,22.4LCl2和HCl的混合气体的物质的量为1mol,含分子总数为6.02×1023,故B错误;
C.0.1mol35Cl原子中含有1.8mol中子,含中子数为1.8×6.02×1023,故C错误;
D.30g甲醛的物质的量为1mol,1mol甲醛含有16mol电子,含有电子数为16×6.02×1023,故D错误;
故选A.
B.准状况下,22.4LCl2和HCl的混合气体的物质的量为1mol,含分子总数为6.02×1023,故B错误;
C.0.1mol35Cl原子中含有1.8mol中子,含中子数为1.8×6.02×1023,故C错误;
D.30g甲醛的物质的量为1mol,1mol甲醛含有16mol电子,含有电子数为16×6.02×1023,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数判断,题目难度中等,注意掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间关系,选项A为易错点,注意铝离子的水解情况.

练习册系列答案
相关题目
测定Cu(NO3)2?nH2O的结晶水含量,下列方案中肯定不可行的是( )
| A、称量样品→加热→冷却→称量CuO |
| B、称量样品→加热→冷却→称量Cu(NO3)2 |
| C、称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量 |
| D、称量样品→加NaOH→过滤→加热→冷却→称量CuO |
对于反应KMn04+HCl→KC1+MnCl2+Cl2↑+H20(未配平)若有0.1mol KMn04 参加反应,下列说法正确的是( )
| A、转移0.5 mol电子 |
| B、生成0.5 mol Cl2 |
| C、参加反应的HC1为1.6 mol |
| D、Cl2是还原产物 |
碘是人体必需的微量元素之一,有“智力元素”之称.我国政府规定,市场供应的食盐必须是加碘食盐,加碘盐中的碘是以哪种物质的形式加入的( )
| A、I2 |
| B、KIO3 |
| C、KI |
| D、以上都不正确 |
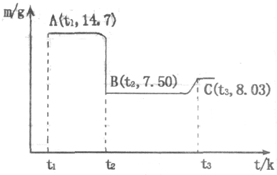
 在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是( )
在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是( )| A、从反应开始到第一次达到平衡时,A物质的平均反应速率为0.667mol/(L?min) |
| B、该反应的化学方程式为2D(s)?2A(g)+B(g)该反应的平衡常数表达式为K=c2(A)?c(B) |
| C、已知反应的△H>0,则第5分钟时图象呈现上述变化的原因可能是升高体系的温度 |
| D、若在第7分钟时增加D的物质的量,则表示A的物质的量变化正确的是b曲线 |
1体积气态烃和2体积氯化氢恰好完全发生反应后,其产物最多还能和8体积氯气发生取代反应,由此可以推断原气态烃是(气体体积均在相同条件下测定)( )
| A、乙炔 | B、1,3-丁二烯 |
| C、戊炔 | D、丙炔 |
某5.6g不纯的铁片(含有下列一种金属)与足量的稀盐酸反应,放出0.21g氢气,则铁片中含有的金属杂质可能是( )
| A、Zn | B、Ag | C、Al | D、Cu |