题目内容
对于反应KMn04+HCl→KC1+MnCl2+Cl2↑+H20(未配平)若有0.1mol KMn04 参加反应,下列说法正确的是( )
| A、转移0.5 mol电子 |
| B、生成0.5 mol Cl2 |
| C、参加反应的HC1为1.6 mol |
| D、Cl2是还原产物 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:根据氧化还原反应中氧化剂和还原剂得失电子数目相等可知反应的方程式为2KMnO4+16HCl=2KC1+2MnCl2+5Cl2+8H2O,根据元素化合价的变化判断氧化剂和还原剂以及电子转移的数目.
解答:
解:配平后的反应的方程式为2KMnO4+16HCl=2KC1+2MnCl2+5Cl2+8H2O,若有0.1molKMnO4 参加反应,则
A.转移电子的物质的量为0.1mol×(7-2)=0.5mol,故A正确;
B.由方程式可知,若有0.1molKMnO4 参加反应,则生成0.25 mol Cl2,故B错误;
C.由方程式可知,若有0.1molKMnO4 参加反应,应有0.8molHCl参加反应,故C错误;
D.反应中HCl被氧化为Cl2,则氧化产物为Cl2,故D错误.
故选A.
A.转移电子的物质的量为0.1mol×(7-2)=0.5mol,故A正确;
B.由方程式可知,若有0.1molKMnO4 参加反应,则生成0.25 mol Cl2,故B错误;
C.由方程式可知,若有0.1molKMnO4 参加反应,应有0.8molHCl参加反应,故C错误;
D.反应中HCl被氧化为Cl2,则氧化产物为Cl2,故D错误.
故选A.
点评:本题考查氧化还原反应,题目难度中等,先配平反应的化学方程式为解答该题的关键,注意氧化剂和还原剂等概念的判断.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
下列实验设计、操作或实验现象均正确的是( )
| A、检验甲酸中是否混有甲醛,可向样品中加入足量NaOH溶液以中和HCOOH,再做银镜反应实验 |
| B、实验室制取乙酸乙酯时,将反应产生的蒸气经导管通入到饱和烧碱溶液中 |
| C、液态溴乙烷中加入AgNO3溶液观察有无淡黄色沉淀生成,以检验溴元素的存在 |
| D、实验室制硝基苯要在水浴的热水中插入温度计 |
关于氧化还原反应10AgF+5C12+5H2O═9口+AgClO3+10HF+O2,下列说法不正确的是( )
| A、每生成1 mol O2,该反应转移电子的物质的量是4NA | ||
| B、该反应中Cl2既是氧化剂,又是还原剂 | ||
| C、口中的物质是AgCl | ||
D、该反应消耗的水有
|
用相同物质的量浓度的盐酸、硫酸、磷酸溶液,分别中和体积相同,浓度相同的氢氧化钠溶液生成正盐,消耗这三种酸的体积比是( )
| A、1:1:1 |
| B、3:2:1 |
| C、6:3:2 |
| D、1:2:3 |
下列最易使酸性高锰酸钾溶液褪色的是( )
A、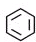 |
B、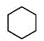 |
C、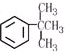 |
D、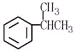 |
为了减慢金属铁的腐蚀,宜采取的措施是( )
①在金属表面涂油
②在金属表面烤漆
③在金属表面镀锌
④将金属放在干燥处
⑤将金属放在潮湿处.
①在金属表面涂油
②在金属表面烤漆
③在金属表面镀锌
④将金属放在干燥处
⑤将金属放在潮湿处.
| A、①②③④ | B、②③⑤ |
| C、③④⑤ | D、①②⑤ |
一瓶无色气体,可能含有HCl、H2S、SO2、HBr、CO2中的一种或几种,将其通入足量氯水中,得无色透明溶液.将该溶液分成两份,一份加盐酸酸化的BaCl2溶液,析出白色沉淀;另一份加硝酸酸化的硝酸银溶液,也有白色沉淀生成.下面结论正确的是 ( )
①原气体中肯定有SO2
②原气体中可能有SO2
③原气体中肯定无H2S、HBr
④不能肯定是否含有HCl
⑤原气体中肯定不含CO2
⑥原气体中肯定含HCl.
①原气体中肯定有SO2
②原气体中可能有SO2
③原气体中肯定无H2S、HBr
④不能肯定是否含有HCl
⑤原气体中肯定不含CO2
⑥原气体中肯定含HCl.
| A、①③④ | B、①④⑤ |
| C、①③⑥ | D、①③④⑤⑥ |
下列说法正确的是( )
| A、200mL1mol/LAl2(SO4)3溶液中,Al3+和SO42-离子总数小于6.02×1023 |
| B、标准状况下,22.4LCl2和HCl的混合气体中含分子总数为2×6.02×1023 |
| C、0.1mol35Cl原子中含中子数为3.5×6.02×1023 |
| D、30g甲醛(CH2O)中共含有电子数为4×6.02×1023 |