题目内容
a、b、c、d四个集气瓶中装有Cl2、H2、HCl、HBr中的一种气体,若a、d两瓶气体混合见光爆炸,a、b两瓶气体混合瓶壁出现暗红色小液滴,则c瓶装的气体是( )
| A、HBr |
| B、HCl |
| C、Cl2 |
| D、H2 |
考点:常见气体的检验
专题:物质检验鉴别题
分析:a、b、c、d四个集气瓶中装有Cl2、H2、HCl、HBr中的一种气体,若a、d两瓶气体混合见光爆炸,则a、d一定为Cl2、H2;
a、b两瓶气体混合瓶壁出现暗红色小液滴,该暗红色小液滴为溴单质,则a、b为Cl2和HBr;
没有涉及的气体只能为c HCl,据此进行解答.
a、b两瓶气体混合瓶壁出现暗红色小液滴,该暗红色小液滴为溴单质,则a、b为Cl2和HBr;
没有涉及的气体只能为c HCl,据此进行解答.
解答:
解:a、d两瓶气体混合见光爆炸,必为H2和Cl2,而a、b两瓶气体混合瓶壁出现暗红色小液滴(液溴),必为Cl2和HBr(发生反应Cl2+2HBr═2HCl+Br2),则a为Cl2,所以d为H2、b为HBr,剩下的c中必盛有HCl,
故选B.
故选B.
点评:本题考查了常见气体的性质及检验方法,题目难度不大,注意掌握常见气体的化学性质及正确的检验方法,正确分析气体间相互反应现象“混合见光爆炸”、生成产物的物理性质“暗红色小液滴”为解答本题的关键.

练习册系列答案
相关题目
常温下,两种气态烃组成的混合气体0.1mol,完全燃烧得0.15mol CO2和3.6g H2O,下列关于该混合气体的说法正确的是( )
①一定有甲烷 ②可能有乙烷 ③一定没有乙烷 ④可能有乙烯.
①一定有甲烷 ②可能有乙烷 ③一定没有乙烷 ④可能有乙烯.
| A、①② | B、①②④ |
| C、①③④ | D、②④ |
下列离子方程式正确的是( )
A、NH4HSO4溶液中加入足量Ba(OH)2溶液:H++SO
| ||
B、在NaHCO3溶液中加入过量Ba(OH)2:2HCO
| ||
| C、Ca(ClO)2溶液中通入过量的CO2气体:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO | ||
D、向NaAlO2溶液中加入HCl至溶液呈酸性:AlO
|
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 除去HC1中含有的少量Cl2 |
B、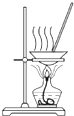 将硫酸铜溶液蒸干,制备蓝矾 |
C、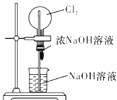 可以完成“喷泉”实验 |
D、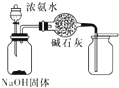 制取并收集干燥纯净的NH3 |
①乙烷、②乙烯、③乙炔、④苯四种烃中,碳原子之间键长由长到短的顺序是( )
| A、①>②>③>④ |
| B、②>①>③>④ |
| C、①>④>②>③ |
| D、④>③>②>① |
由粗硅制纯硅的反应中,氯气起了什么作用( )
| A、把硅氧化为四氯化硅 |
| B、把二氧化硅还原为硅 |
| C、把石英砂中的杂质氧化除去 |
| D、以上都不对 |
Se是人体必需微量元素,下列有关
Se和
Se的说法正确的是( )
78 34 |
80 34 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
下列说法正确的是( )
| A、硫可溶于水 |
| B、硫易溶于二硫化碳 |
| C、硫单质在与Cu、Fe、O2的反应中均作氧化剂 |
| D、硫在自然界中仅以化合态存在 |