题目内容
下述四个反应中,酸所体现的性质与其他三者明显不同的是( )
| A、浓盐酸与二氧化锰共热制氯气 |
| B、浓硫酸与铜片加热 |
| C、浓硝酸与铜反应 |
| D、稀硝酸与铜反应 |
考点:氯、溴、碘及其化合物的综合应用,硝酸的化学性质,浓硫酸的性质
专题:
分析:A.盐酸作还原剂和酸;
B.浓硫酸作酸和氧化剂;
C.浓硝酸作氧化剂和酸;
D.稀硝酸作氧化剂和酸.
B.浓硫酸作酸和氧化剂;
C.浓硝酸作氧化剂和酸;
D.稀硝酸作氧化剂和酸.
解答:
解:A.由MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O可知,Cl元素的化合价升高,还生成氯化锰,则盐酸作还原剂和酸;
B.由Cu+2H2SO4=(浓)
CuSO4+SO2↑+2H2O可知,S元素的化合价降低,还生成硫酸铜,则硫酸作氧化剂和酸;
C.由Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O可知,N元素的化合价降低,还生成硝酸铜,则硝酸作氧化剂和酸;
D.由3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O可知,N元素的化合价降低,还生成硝酸铜,则硝酸作氧化剂和酸,
显然A中酸所体现的性质与其他三者明显不同,
故选A.
| ||
B.由Cu+2H2SO4=(浓)
| ||
C.由Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O可知,N元素的化合价降低,还生成硝酸铜,则硝酸作氧化剂和酸;
D.由3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O可知,N元素的化合价降低,还生成硝酸铜,则硝酸作氧化剂和酸,
显然A中酸所体现的性质与其他三者明显不同,
故选A.
点评:本题考查酸的性质及氧化还原反应,为高频考点,把握发生的反应及元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意生成盐体现酸性,题目难度不大.

练习册系列答案
相关题目
以下能级符号不正确的是( )
| A、6s | B、2d | C、5f | D、7p |
卤代烃R-CH2-CH2-X中的化学键如下图所示,则下列说法正确的是( )

| A、该卤代烃发生水解反应时,被破坏的键是①和② |
| B、该卤代烃发生消去反应时,被破坏的键是①和④ |
| C、该卤代烃发生取代反应时,被破坏的键是① |
| D、该卤代烃发生消去反应时,被破坏的键是①和② |
某未知溶液可能含Cl-、CO32-、Na+、SO42-、Al3+,将溶液滴在蓝色石蕊试纸上,试纸变红.取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀.下列判断合理的是①一定有Cl-,②一定有SO42-,③一定没有Al3+,④一定没有CO32-.( )
| A、①② | B、③④ | C、①③ | D、②④ |
下列运用电解法生产产品的说法错误的是( )
| A、铝厂通过电解熔融氧化铝的方法冶炼铝 |
| B、制钠厂通过电解熔融氯化钠的方法生产金属钠 |
| C、用电解饱和食盐水的方法生产烧碱,同时得到氯气和氢气 |
| D、制钠厂通过电解饱和食盐水的方法生产金属钠 |
配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A、称量时NaOH已经潮解 |
| B、定容时俯视容量瓶的标线 |
| C、向容量瓶中转移溶液时,容量瓶事先用蒸馏水洗涤过 |
| D、摇匀后发现液面低于标线,滴加蒸馏水至标线再摇匀 |
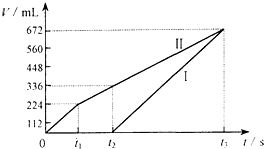 常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算: