题目内容
4. 铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读如图,K闭合时下列判断不正确的是( )
铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读如图,K闭合时下列判断不正确的是( )| A. | d电极:PbSO4+2H2O-2e-=PbO2+4H++SO42- | |
| B. | 当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol | |
| C. | Ⅱ中SO42-向c电极迁移 | |
| D. | K闭合一段时间后,Ⅱ可单独作为原电池,d电极为正极 |
分析 K闭合时,Ⅰ装置是原电池,Ⅱ是电解池,则a为正极、b为负极、c为阴极、d为阳极,以此可书写电极反应式,其中b电极反应为Pb-2e-+SO42-=PbSO4 ,a电极反应为PbO2+2e-+4H++SO42-=PbSO4+2H2O,c电极反应为PbSO4+2e-=Pb+SO42-,d电极方程式为PbSO4+2H2O-2e-=PbO2+4H++SO42-,以此解答该题.
解答 解:A.K闭合时Ⅰ为原电池,Ⅱ为电解池,Ⅱ中发生充电反应,d电极为阳极发生氧化反应,其反应式为PbSO4+2H2O-2e-=PbO2+4H++SO42-,故A正确;
B.在Ⅰ装置总反应式中Pb+PbO2+2H2SO4=2H2O+2PbSO4,得失电子总数为2e-,当电路中转移0.2mol电子时,可以计算出Ⅰ中消耗的硫酸的量为0.2mol,故B正确;
C.当k闭合时Ⅰ为原电池,Ⅱ为电解池,Ⅱ中c电极上的PbSO4转化为Pb和SO2-4,d电极上的PbSO4转化为PbO2和SO42-,故SO42-从两极上脱离下来向四周扩散而并非做定向移动,故C错误;
D.K闭合一段时间,也就是充电一段时间后Ⅱ可以作为原电池,由于c表面生成Pb,放电时做电源的负极,d表面生成PbO2,做电源的正极,故D正确.
故选C.
点评 本题综合考查原电池和电解池知识,注意把握电极反应式的书写,为解答该题的关键,学习中要把握原电池和电解池的工作原理.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如表:A的气态氢化物能使湿润的红色石蕊试纸变蓝;C单质在实验室一般保存在煤油中;F的最高价氧化物对应水化物既能和酸反应又能和强碱反应,G单质是日常生活中用量最大的金属,易被腐蚀.请回答下列问题: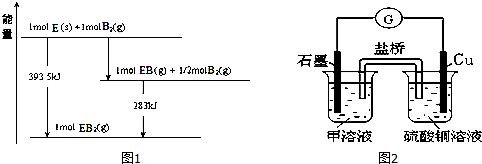
(1)A元素在周期表中的位置是第二周期第VA族.
(2)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中可能引起的环境问题有:(任写一种)酸雨或光化学烟雾;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若使所得溶液pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2 (g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.某同学假设正极产物是Fe2+,请你设计实验证明该假设滴加酸性高锰酸钾溶液,若溶液紫色褪去(或滴加铁氰化钾溶液,产生蓝色沉淀),则产品中含有Fe2+.

| … | E | A | B | ||
| C | … | D |
(2)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中可能引起的环境问题有:(任写一种)酸雨或光化学烟雾;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若使所得溶液pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2 (g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.某同学假设正极产物是Fe2+,请你设计实验证明该假设滴加酸性高锰酸钾溶液,若溶液紫色褪去(或滴加铁氰化钾溶液,产生蓝色沉淀),则产品中含有Fe2+.
12.下列事实中,不能用平衡移动原理解释的是( )
| A. | 开启啤酒瓶后,瓶中马上泛起大量泡沫 | |
| B. | 对CO(g)+NO2(g)═CO2(g)+NO(g)平衡体系增大压强可使其颜色变深 | |
| C. | 常温下,将1mLpH=3的醋酸溶液加水稀释到100mL,测得其pH<5 | |
| D. | 实验室中常用排饱和食盐水的方法收集氯气 |
19.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | Kw/c(H+)=1 mol•L-1的溶液中:Na+、SiO32-、I-、CO32- | |
| B. | 氨水中:Al3+、K+、F-、NO3- | |
| C. | pH=1的溶液中:NH4+、Na+、SO42-、CH3COO- | |
| D. | 0.1 mol•L-1的NaHSO4溶液中:K+、Fe2+、Cl-、NO3- |
16.天津港爆炸现场的氰化钠有剧毒,用过氧化氢处理含氰废水的第一步反应原理如下:CN-+H2O2$\frac{\underline{\;催化剂\;}}{\;}$CNO-+H2O.下列说法正确的是( )
| A. | 反应中H2O2被氧化 | |
| B. | CNO-中N的化合价为-3价 | |
| C. | 温度越高越有利于该反应发生 | |
| D. | 每生成1.8 g H2O,转移电子数为0.4NA |
13.下列实验操作中,错误的是( )
| A. | 蒸馏操作时,冷凝水的方向应当由下往上 | |
| B. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| C. | 蒸馏时,应使温度计水银球位于蒸馏烧瓶的支管口处 | |
| D. | 分液操作时,首先要打开分液漏斗的上口瓶塞,或使瓶塞上的凹槽与上口部的小孔对准,然后进行分液 |
 .
. .
. .
.