题目内容
13.下列实验操作中,错误的是( )| A. | 蒸馏操作时,冷凝水的方向应当由下往上 | |
| B. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| C. | 蒸馏时,应使温度计水银球位于蒸馏烧瓶的支管口处 | |
| D. | 分液操作时,首先要打开分液漏斗的上口瓶塞,或使瓶塞上的凹槽与上口部的小孔对准,然后进行分液 |
分析 A.冷凝管中水的方向采用逆向通水法,即下口为进水口,上口是出水口;
B.萃取与密度大小无关;
C.蒸馏时,温度计用于测量馏分的温度;
D.在分液操作时,必须使分液漏斗内外空气相通.
解答 解:A.蒸馏操作时,冷凝管中水的方向是下口为进水口,上口是出水口,保证气体与水充分接触,即冷凝水的方向应当由下往上,故A正确;
B.萃取与溶质在不同溶剂中的溶解度有关,则利用溶质在两种互不相溶的溶剂中溶解度的不同,使溶质从一种溶剂内转移到另一种溶剂的操作为萃取,与密度大小无关,故B错误;
C.蒸馏时,测定馏分的温度,则应调整温度计的水银球于蒸馏烧瓶支管口附近,故C正确;
D.分液操作时,首先要打开分液漏斗的上口活塞,或使活塞上的小孔与上口部的小孔对准,使内外空气相通,保证液体顺利流出,故D正确.
故选B.
点评 本题考查化学实验方案的评价、化学基本操作方法及其综合应用,侧重于物质的分离、提纯的考查,题目难度中等,注意把握物质的性质的异同以及分离的原理、操作方法,为高频考点,注意相关基础知识的积累.

练习册系列答案
相关题目
4. 铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读如图,K闭合时下列判断不正确的是( )
铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读如图,K闭合时下列判断不正确的是( )
 铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读如图,K闭合时下列判断不正确的是( )
铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读如图,K闭合时下列判断不正确的是( )| A. | d电极:PbSO4+2H2O-2e-=PbO2+4H++SO42- | |
| B. | 当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol | |
| C. | Ⅱ中SO42-向c电极迁移 | |
| D. | K闭合一段时间后,Ⅱ可单独作为原电池,d电极为正极 |
8.下列说法不正确的是( )
| A. | 由于电流的作用,酸、碱、盐溶于水发生电离 | |
| B. | 胶体的分散质粒子直径小于l00nm但大于1nm,能通过滤纸,不能透过半透膜 | |
| C. | 存在自由移动的离子是电解质溶液导电的原因 | |
| D. | 向氢氧化铁胶体中滴加稀硫酸,开始时产生沉淀,继续滴加时沉淀溶解 |
18.2H2S+SO2═3S↓+2H2O的反应中,当有4×6.02×1023个电子发生转移时,得到的氧化产物比还原产物多( )
| A. | 64 g | B. | 32 g | C. | 1.5mol | D. | 3 mol |
2.根据如图海水综合利用的工业流程图,判断下列说法正确的是.( )
已知:MgCl2.6H2O受热生成Mg(OH) Cl和HC1气体等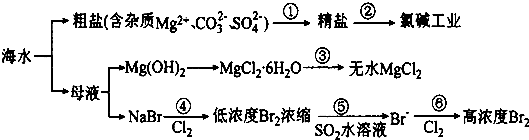
已知:MgCl2.6H2O受热生成Mg(OH) Cl和HC1气体等

| A. | 过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 | |
| B. | 过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 | |
| C. | 在过程④、⑥反应中每氧化0.2 mol Br一需消耗2.24LCl2 | |
| D. | 在过程③中将MgCl2.6H2O灼烧即可制得无水MgCl2 |