题目内容
在一固定容积的密闭容器中,保持一定温度,在一定条件下进行以下反应:A(g)+2B(g)?3C(g),已知加入1mol A和3mol B且达到平衡后,生成了a mol C.
(1)达到平衡时,C在反应混合气中的体积分数是 %(用含字母a的代数式表示).
(2)在相同实验条件下,若在同一容器中改为加入2mol A和6mol B,达到平衡后,C的物质的量为 mol(用含字母a的代数式表示).
(3)在相同实验条件下,若在同一容器中改为加入2mol A和8mol B,若要求平衡后C在反应混合气中体积分数仍与原平衡相同,则还应加入C mol.
(1)达到平衡时,C在反应混合气中的体积分数是
(2)在相同实验条件下,若在同一容器中改为加入2mol A和6mol B,达到平衡后,C的物质的量为
(3)在相同实验条件下,若在同一容器中改为加入2mol A和8mol B,若要求平衡后C在反应混合气中体积分数仍与原平衡相同,则还应加入C
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)先利用反应前后气体体积不变,求出平衡时混合气体的总的物质的量,再根据体积分数定义计算;
(2)恒温恒容,反应前后气体体积不变,对应物质按相同的比例加入,平衡等效,物质的转化率相同,平衡时对应组分的含量相同;
(3)积分数仍与原平衡相同,说明为等效平衡,恒温恒容,反应前后气体体积不变,按化学计量数转化到左边,A、B的物质的量之比满足1:3,则与原平衡等效.
(2)恒温恒容,反应前后气体体积不变,对应物质按相同的比例加入,平衡等效,物质的转化率相同,平衡时对应组分的含量相同;
(3)积分数仍与原平衡相同,说明为等效平衡,恒温恒容,反应前后气体体积不变,按化学计量数转化到左边,A、B的物质的量之比满足1:3,则与原平衡等效.
解答:
解:(1)反应前后气体体积不变,所以平衡时混合气体的总的物质的量为1mol+3mol=4mol,所以平衡时,C在反应混合气中的体积分数为
×100%=25a%,
故答案为:25a%;
(2)恒温恒容,反应前后气体体积不变,加入2molA和6molB,A、B的物质的量之比为1:3,与原平衡相同,为等效平衡,物质的转化率相同,平衡时对应组分的含量相同,C在反应混合气中的体积分数不变,C的物质的量变为2amol,故答案为:2a;
(3)恒温恒容,反应前后气体体积不变,按化学计量数转化到左边,A、B的物质的量之比满足1:3,
令加入nmolC,则:
=
,解得n=6,故答案为:6.
| amol |
| 4mol |
故答案为:25a%;
(2)恒温恒容,反应前后气体体积不变,加入2molA和6molB,A、B的物质的量之比为1:3,与原平衡相同,为等效平衡,物质的转化率相同,平衡时对应组分的含量相同,C在反应混合气中的体积分数不变,C的物质的量变为2amol,故答案为:2a;
(3)恒温恒容,反应前后气体体积不变,按化学计量数转化到左边,A、B的物质的量之比满足1:3,
令加入nmolC,则:
2mol+
| ||
8mol+
|
| 1 |
| 3 |
点评:本题考查化学平衡计算及等效平衡,难度中等,理解等效平衡规律:
1、恒温恒容,反应前后气体体积不等,按化学计量数转化一边,对应物质满足等量;反应前后气体体积相等,按化学计量数转化一边,对应物质满足对比.
2:恒温恒压,按化学计量数转化一边,对应物质满足对比;题目难度中等.
1、恒温恒容,反应前后气体体积不等,按化学计量数转化一边,对应物质满足等量;反应前后气体体积相等,按化学计量数转化一边,对应物质满足对比.
2:恒温恒压,按化学计量数转化一边,对应物质满足对比;题目难度中等.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
常温下,下列有关电解质溶液的叙述正确的是( )
| A、等浓度等体积的强酸与强碱溶液混合后,溶液的pH=7 |
| B、将10 mL pH=a的盐酸与100 mL pH=b的Ba(OH)2溶液混合后恰好中和,则a+b=13 |
| C、pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合后溶液的pH=10.7(已知lg 2=0.3) |
| D、pH=2的盐酸与pH=12的氨水等体积混合后所得溶液显中性 |
下列说法正确的是( )
A、已知
| ||||||||||
B、常温下
| ||||||||||
| C、在复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是:NH4++Fe3++2SO42-+2Ba2++4OH-═2BaSO4↓+Fe(OH)3↓+NH3?H2O | ||||||||||
| D、向浓度均为0.1 mol/L的MgCl2、CuCl2混合溶液中逐滴加入氨水,先生成Cu(OH)2沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2] |
常温下,浓度均为0.1 mol?L-1CH3COOH溶液和HCN溶液的pH分别为m和n(1<m<n).下列叙述中错误的是( )
| A、常温下,pH相同的CH3COOH溶液和HCN溶液分别加水稀释相同的倍数时,前者pH变化较小 |
| B、等温下,等浓度的CH3COOH和HCN溶液pH,后者大 |
| C、HCN溶液和NaOH不等体积混合后一定存在如下关系c(H+)-c(OH-)═c(CN-)-c(Na+) |
| D、0.1mol?L-1CH3COOH和HCN溶液中由水电离出的c(H+),前者是后者的10m-n倍 |
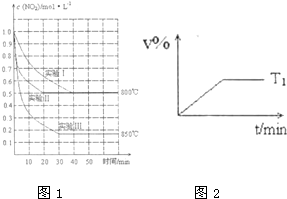 体积为2L的密闭容器中反应2NO2(g)?2NO(g)+O2(g)在三种不同条件下进行,其中实验I、II都在800℃、实验III在850℃;NO、O2的起始浓度都为0,NO2 的浓度随时间的变化如图所示.请回答下列问题:
体积为2L的密闭容器中反应2NO2(g)?2NO(g)+O2(g)在三种不同条件下进行,其中实验I、II都在800℃、实验III在850℃;NO、O2的起始浓度都为0,NO2 的浓度随时间的变化如图所示.请回答下列问题: 以乙烯为原料合成化合物C的流程如图所示:
以乙烯为原料合成化合物C的流程如图所示: