题目内容
用来表示可逆反应2A(g)+B(g)?2C(g);△H<0的正确图象为( )
A、 |
B、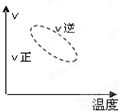 |
C、 |
D、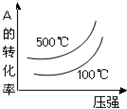 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:由反应方程式可知,升高温度,正逆反应速率都增大,由于正反应放热,平衡向逆反应方向移动,C的含量降低,A的转化率降低,C的百分含量增大.
解答:
解:A、正反应放热,升高温度,根据平衡移动原理,平衡向逆反应方向移动,C的含量降低,与图象吻合,故A正确;
B、升高温度,正逆反应速率都增大,与图象不符,故B错误;
C、增大压强,正逆反应速率都增大,但图中逆反应速率逐渐减小,与图象不符,故C错误;
D、根据平衡移动原理,增大压强,平衡向正反应方向移动,A的转化率减小,但图象增大,升高温度,平衡向逆反应方向移动,A的转化率减小,但图象增大.
故选:A.
B、升高温度,正逆反应速率都增大,与图象不符,故B错误;
C、增大压强,正逆反应速率都增大,但图中逆反应速率逐渐减小,与图象不符,故C错误;
D、根据平衡移动原理,增大压强,平衡向正反应方向移动,A的转化率减小,但图象增大,升高温度,平衡向逆反应方向移动,A的转化率减小,但图象增大.
故选:A.
点评:本题主要考查你对影响化学平衡的因素,影响化学反应速率的因素等考点的理解.

练习册系列答案
相关题目
在盛有水的电解槽中加入等物质的量的Ag+,Pb2+,K+,SO42-,NO3-,Cl-,然后用惰性电极电解,通电片刻后,所得氧化产物和还原产物的质量之比为( )
| A、1:2 | B、8:1 |
| C、16:207 | D、71:216 |
下列实验操作正确的是( )
| A、粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌过滤器中的液体 |
| B、容量瓶检漏:在容量瓶中注入适量的水,塞上玻璃瓶塞,左手五指托住瓶底,右手食指顶住瓶塞,反复倒置数次,观察是否漏水 |
| C、用分液法分离C2H5OH与H2O的混合物 |
| D、测定溶液pH的操作:将pH试纸置于表面皿上,用玻璃棒蘸取溶液,点在pH试纸的中部,与对应的标准比色卡比较 |
在CH3COONa溶液中,各微粒的浓度关系错误的是( )
| A、c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B、c(OH-)=c(H+)+c(CH3COOH) |
| C、c(Na+)=c(CH3COO-)+c(CH3COOH) |
| D、c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
洗涤BaSO4固体中吸附的Na+和Cl-,最好用下列试剂中的( )
| A、BaCl2溶液 |
| B、稀H2SO4 |
| C、Na2SO4溶液 |
| D、蒸馏水 |
 2CO2(g)+N2(g)△H<0
2CO2(g)+N2(g)△H<0

 A、B、C、D是中学化学常见的四种物质,它们的转化关系如下:A+B=C+D
A、B、C、D是中学化学常见的四种物质,它们的转化关系如下:A+B=C+D