题目内容
8.已知反应A+B=C+D的能量变化如图所示,下列说法不正确的是( )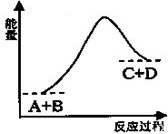
| A. | 只有在加热条件下该反应才能进行 | |
| B. | 该反应是吸热反应 | |
| C. | 反应物的总能量低于生成物的总能量 | |
| D. | 反应中断开化学键吸收的总能量高于形成化学键放出的总能量 |
分析 化学上把有热量放出的反应叫做放热反应,把吸收热量的反应叫做吸热反应,从图象可见,反应物能量低于生成物能量,反应吸热.
解答 解:A、吸热反应不一定需要加热,如氯化铵和氢氧化钡反应吸热,不需要任何条件,故A错误;
B、反应物能量大于生成物,反应吸热,故B正确;
C、生成物能量高于反应物,故C正确;
D、反应吸热,反应物键能大于生成物键能和,反应中断开化学键吸收的总能量高于形成化学键放出的总能量,故D正确;
故选A.
点评 本题考查吸热反应和放热反应的区别,主要是图象分析、物质能量大小比较、反应实质的理解应用,题目难度不大.

练习册系列答案
相关题目
19.实验室用锌与稀硫酸反应制取H2,欲使产生H2的速率加快,下列措施可行的是( )
| A. | 加水稀释 | B. | 加少量NaOH溶液 | C. | 改用98%的浓硫酸 | D. | 锌片改为锌粒 |
16.下列各组有机物中,仅使用溴水不 能鉴别出的是( )
| A. | 苯和四氯化碳 | B. | 乙醇和乙酸 | C. | 乙烷和乙烯 | D. | 苯和酒精 |
3.下列物质中:①SO2 ②丙烯 ③丙烯酸 ④苯酚 ⑤HI ⑥HCHO跟溴水、酸性高锰酸钾溶液、碳酸氢钠溶液都能发生反应的是( )
| A. | ⑤⑥ | B. | ①②④⑥ | C. | ①③ | D. | ①③⑤ |
13.下列反应可用于设计原电池的是( )
| A. | CO2+2H2O═CH4+2O2 | B. | NaOH+HCl═NaCl+H2O | ||
| C. | 4Al+3O2+6H2O═4Al(OH)3 | D. | Cu+2HCl═CuCl2+H2↑ |
20.某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )

| A. | b、c三点溶液的离子浓度之和c>b>a | |
| B. | b点溶液中c(H+)+c(NH3•H2O)=(OH-) | |
| C. | 用等浓度的NaOH溶液和等体积b、c处溶液反应,恰好反应时消耗NaOH溶液的体积Vb=Vc | |
| D. | a、b、c三点溶液中水的电离程度a>b>c |
17.下列关于同分异构体、同系物的说法和判断中,正确的是( )
| A. | C2H4和C3H6一定属于同系物 | |
| B. | 淀粉[(C6H10O5)n]与纤维素[(C6H10O5)n]互为同分异构体 | |
| C. | 同系物之间化学性质相似,物理性质递变 | |
| D. | 同分异构体之间化学性质相似,物理性质递变 |
18.回答下列问题
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
①某同学根据上述信息,推断B的核外电子排布如图1所示,该同学所画的电子排布图违背能量最低原理,B元素位于周期表五个区域中的s区

②ACl2分子中A的杂化类型为sp杂化,ACl2的空间构型为直线形.
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物.
①以体心立方堆积形成的金属铁中,其原子的配位数为8.
②写出一种与CN-互为等电子体的单质的电子式 .
.
③六氰合亚铁离子[Fe(CN)6]4-中不存在B.
A.共价键 B.非极性键 C.配位键 D.σ键 E.π键
(3)一种Al-Fe合金的立体晶胞如图2所示.请据此回答下列问题:
①确定该合金的化学式Fe2Al.
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为$\root{3}{\frac{139}{2ρ{N}_{A}}}$cm.
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15399 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |

②ACl2分子中A的杂化类型为sp杂化,ACl2的空间构型为直线形.
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物.
①以体心立方堆积形成的金属铁中,其原子的配位数为8.
②写出一种与CN-互为等电子体的单质的电子式
 .
.③六氰合亚铁离子[Fe(CN)6]4-中不存在B.
A.共价键 B.非极性键 C.配位键 D.σ键 E.π键
(3)一种Al-Fe合金的立体晶胞如图2所示.请据此回答下列问题:
①确定该合金的化学式Fe2Al.
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为$\root{3}{\frac{139}{2ρ{N}_{A}}}$cm.