题目内容
下列叙述中正确的是( )
| A、热化学方程式中,各物质前的化学计量数不表示分子个数 |
| B、如果反应物所具有的总能量小于生成物所具有的总能量,则发生的反应是放热反应 |
| C、在稀溶液中,1 mol酸和1 mol碱完全反应所放出的热量,叫做中和热 |
| D、在101 kPa时,1 mol物质燃烧时所放出的热量叫做该物质的燃烧热 |
考点:热化学方程式,燃烧热,中和热
专题:化学反应中的能量变化
分析:A.热化学方程式中的化学计量数只表示物质的量,不表示微粒数,所以系数可以用分数表示;
B.如果放热反应中反应物所具有的总能量大于生成物所具有的总能量;
C.根据中和热的概念分析;
D.根据燃烧热的概念分析.
B.如果放热反应中反应物所具有的总能量大于生成物所具有的总能量;
C.根据中和热的概念分析;
D.根据燃烧热的概念分析.
解答:
解:A.热化学方程式中,各物质前的化学计量数不表示分子个数,只表示物质的量,故A正确;
B.如果反应物所具有的总能量大于生成物所具有的总能量,则发生的反应是放热反应,故B错误;
C.中和热是强酸与强碱的稀溶液发生中和反应生成1mol水时放出的热量,故C错误
D.燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,DB错误;
故选A.
B.如果反应物所具有的总能量大于生成物所具有的总能量,则发生的反应是放热反应,故B错误;
C.中和热是强酸与强碱的稀溶液发生中和反应生成1mol水时放出的热量,故C错误
D.燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,DB错误;
故选A.
点评:本题主要考查了燃烧热、中和热以及热化学方程式等,难度不大,注意概念的掌握.

练习册系列答案
相关题目
100mL 6mol?L-1的H2SO4跟过量的锌反应,在一定温度下,为减缓反应速率,但又不影响生成氢气的总量,可向反应物中加入少量的( )
| A、硫酸钠固体 |
| B、醋酸钠固体 |
| C、硫酸铜溶液 |
| D、硝酸钾溶液 |
在可逆反应2SO2+O2?2SO3的平衡状态下,保持恒温恒容向容器中加入一定量的O2,下列说法正确的是(K为平衡常数,QC为浓度商)( )
| A、QC不变,K变大,O2转化率增大 |
| B、QC不变,K变大,SO2转化率增大 |
| C、QC变小,K不变,O2转化率减小 |
| D、QC增大,K不变,SO2转化率增大 |
下列说法不正确的是 ( )
| A、由于铜盐能杀死某些细菌,并能抑制藻类生长,因此游泳池馆常用硫酸铜作池水消毒剂 |
| B、明矾溶于水后能生成Al(OH)3胶体,它能凝聚水中的悬浮物并起到杀菌消毒的作用,从而达到净水的目的 |
| C、铝制品表面有致密的氧化膜保护层,所以不能盛放酸、碱溶液,但可以长时间盛放咸菜等腌制品 |
| D、工业电解氧化铝时,向其中添加冰晶石,使氧化铝的熔点降低,从而减少冶炼过程中的能量消耗 |
有关下列物质分子结构特征描述正确的是( )
| A、乙烯分子中碳、氢原子个数比为1:2,证明乙烯分子里含有一个碳碳双键 |
B、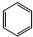 表示苯分子的结构,因此能解释邻二甲苯有 表示苯分子的结构,因此能解释邻二甲苯有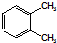 和 和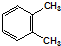 两种结构 两种结构 |
C、因为甲烷是一种正四面体结构,所以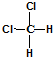 和 和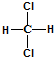 属于同一种物质 属于同一种物质 |
| D、苯的分子式是C6H6,分子式中碳原子远没有饱和,因此苯能使溴水褪色 |
在下列实验操作中:①过滤;②蒸发;③溶解;④取液体试剂;⑤取固体试剂;⑥移液.一定要用到玻璃棒的是( )
| A、①②③④ | B、①②③⑥ |
| C、①③⑤⑥ | D、③④⑤⑥ |