题目内容
某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+.为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁晶体和金属铜.请根据如下回收流程图,回答有关问题: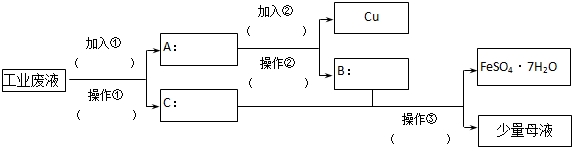
(1)加入①为 ,加入②为 (要考虑用量).
(2)操作②的名称为 .
(3)母液中含有的离子有(填离子符号): .
(4)为了得到纯净的FeSO4?7H2O晶体,操作③在蒸发、冷却结晶后还要洗涤FeSO4?7H2O晶体,洗涤FeSO4?7H2O晶体的方法是: .

(1)加入①为
(2)操作②的名称为
(3)母液中含有的离子有(填离子符号):
(4)为了得到纯净的FeSO4?7H2O晶体,操作③在蒸发、冷却结晶后还要洗涤FeSO4?7H2O晶体,洗涤FeSO4?7H2O晶体的方法是:
考点:物质分离和提纯的方法和基本操作综合应用,物质分离、提纯的实验方案设计
专题:实验设计题
分析:工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+,从该废水中回收硫酸亚铁和金属铜,结合流程可知,①为Fe,操作①为过滤,C为滤液,且C中含FeSO4,则A中含Cu及过量的Fe,加入②为稀硫酸,操作②为过滤,则B中主要含硫酸亚铁,B、C混合液中主要含FeSO4,操作③为蒸发、浓缩、结晶、过滤,可得到FeSO4.7H2O,以此来解答.
解答:
解:工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+,从该废水中回收硫酸亚铁和金属铜,结合流程可知,①为Fe,操作①为过滤,C为滤液,且C中含FeSO4,则A中含Cu及过量的Fe,加入②为稀硫酸,操作②为过滤,则B中主要含硫酸亚铁,B、C混合液中主要含FeSO4,操作③为蒸发、浓缩、结晶、过滤,可得到FeSO4.7H2O,
(1)由上述分析可知,①为过量Fe,②为适量的硫酸,故答案为:过量Fe;适量的硫酸;
(2)由上述分析可知,操作②分离不溶性固体与溶液,则为过滤,故答案为:过滤;
(3)由B、C混合液中主要含FeSO4,可知蒸发、浓缩、结晶、过滤母液中含有的离子有Fe2+、SO42-,故答案为:Fe2+、SO42-;
(4)洗涤FeSO4?7H2O晶体的方法是将晶体转移到过滤器中,沿着玻璃棒加蒸馏水浸没晶体,使水自然流下,重复2~3次即可,故答案为:将晶体转移到过滤器中,沿着玻璃棒加蒸馏水浸没晶体,使水自然流下,重复2~3次即可.
(1)由上述分析可知,①为过量Fe,②为适量的硫酸,故答案为:过量Fe;适量的硫酸;
(2)由上述分析可知,操作②分离不溶性固体与溶液,则为过滤,故答案为:过滤;
(3)由B、C混合液中主要含FeSO4,可知蒸发、浓缩、结晶、过滤母液中含有的离子有Fe2+、SO42-,故答案为:Fe2+、SO42-;
(4)洗涤FeSO4?7H2O晶体的方法是将晶体转移到过滤器中,沿着玻璃棒加蒸馏水浸没晶体,使水自然流下,重复2~3次即可,故答案为:将晶体转移到过滤器中,沿着玻璃棒加蒸馏水浸没晶体,使水自然流下,重复2~3次即可.
点评:本题考查混合物分离提纯的综合应用,为高频考点,把握物质的性质、发生的反应及除杂的原则等为解答的关键,侧重分析、实验能力的考查,注意实验技能的应用,题目难度中等.

练习册系列答案
相关题目
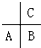 短周期元素A、B、C(均不为稀有气体元素)在周期表中的位置如图:下列说法正确的是( )
短周期元素A、B、C(均不为稀有气体元素)在周期表中的位置如图:下列说法正确的是( )| A、若均为非金属元素,其气态氢化物稳定性:A<B<C |
| B、若均为金属元素,其最高价氧化物的水化物的碱性:A<B<C |
| C、原子半径:A>C>B |
| D、最高正价:A>B>C |
除去粗盐中的Ca2+、Mg2+、SO42-,可将粗盐溶于水后进行如下操作:①过滤,②加过量的NaOH溶液,③加适量的盐酸,④加过量的Na2CO3溶液,⑤加过量的BaCl2溶液,⑥蒸发结晶,其中操作顺序正确的是( )
| A、①②③④⑤⑥ |
| B、②⑤④①③⑥ |
| C、①②④⑤③⑥ |
| D、④②③①⑤⑥ |
下列叙述中正确的是( )
| A、热化学方程式中,各物质前的化学计量数不表示分子个数 |
| B、如果反应物所具有的总能量小于生成物所具有的总能量,则发生的反应是放热反应 |
| C、在稀溶液中,1 mol酸和1 mol碱完全反应所放出的热量,叫做中和热 |
| D、在101 kPa时,1 mol物质燃烧时所放出的热量叫做该物质的燃烧热 |

 如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制200mL 1.0mol/L的稀硫酸.可供选用的仪器有:
如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制200mL 1.0mol/L的稀硫酸.可供选用的仪器有: