题目内容
5.下列有关实验操作及原理正确的是( )| A. | 用玻璃棒蘸取NaClO溶液,点在干燥的pH试纸上,证明HClO是弱酸 | |
| B. | 将一定量的FeCl3晶体、盐酸依次加入容量瓶中,配制一定物质的量浓度的FeCl3溶液 | |
| C. | 将Cu与浓硫酸反应剩余的液体加入到盛有蒸馏水的烧杯中,以证明反应生成了CuSO4 | |
| D. | 用乙醇、乙酸制取乙酸乙酯的过程中发现忘加碎瓷片,可立即补加 |
分析 A.NaClO溶液具有漂白性;
B.不能在容量瓶中溶解固体;
C.硫酸铜溶于水显蓝色;
D.不能在已经加热的液体中补加碎瓷片,防止液体爆沸.
解答 解:A.NaClO溶液具有漂白性,能够使pH试纸褪色,所以不能用pH试纸来测定NaClO溶液的pH,故A错误;
B.不能在容量瓶中溶解固体,应该先把FeCl3晶体、盐酸依次加入烧杯中,再加蒸馏水溶解,然后转移到容量瓶中,故B错误;
C.将Cu与浓硫酸反应剩余的液体加入到盛有蒸馏水的烧杯中,由于硫酸铜溶于水显蓝色,根据溶液的颜色可以证明反应生成了CuSO4,故C正确;
D.不能在已经加热的液体中补加碎瓷片,防止液体爆沸,应该等到混合液体冷却后再向容器中加碎瓷片,故D错误.
故选C.
点评 本题考查较为综合,涉及pH试纸的使用、溶液的配制、物质的检验和鉴别、物质的制备等操作,侧重于学生的实验能力的考查,注意把握物质的性质的异同以及实验的严密性,难度不大.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
15.下列说法中正确的是( )
| A. | 硫是黄色能溶于水的晶体 | |
| B. | 臭氧空洞的形成主要与SO2有关 | |
| C. | 硫在自然界仅以化合态存在 | |
| D. | 硫既能与某些金属反应又能与某些非金属反应 |
16.广泛存在于装修材料和胶合板、涂料中且家庭装修中空气污染源之首的一种有机物是( )
| A. | 二氧化碳 | B. | 二氧化氮 | C. | 氮气 | D. | 甲醛 |
13.下列各组粒子中粒子半径由小到大的是( )
| A. | O2- Na+Mg2+Al3+ | B. | O P S Cl | ||
| C. | A l3+Mg2+ Na+ F- | D. | K+ Mg2+ Al3+ H+ |
10.下列表达式错误的是( )
| A. | 甲烷的电子式: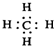 | |
| B. | 氮原子的L层电子的电子排布图: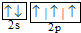 | |
| C. | 碳-12原子:${\;}_{6}^{12}$C | |
| D. | S2-的核外电子排布式:1s22s22p63s23p4 |
17.国际无机化学命名委员会将元素周期表原先的主、副族族号取消,从左往右改为18列,碱金属为第1列,稀有气体为第18列,按这个规定,下列说法不正确的是( )
| A. | 不仅有第2列元素的原子最外层有2个电子 | |
| B. | 第3~12列元素全为金属 | |
| C. | 第3列元素种类最多 | |
| D. | 第16、17列元素都是非金属元素 |
14.关于丙烯醛(CH2=CH-CHO)的下列叙述中,不正确的是( )
| A. | 在丙烯醛分子中,含有两种官能团 | |
| B. | 丙烯醛能发生加聚反应,生成高聚物  | |
| C. | 等物质的量的丙烯醛和丙醛完全燃烧,消耗等物质的量的O2 | |
| D. | 丙烯醛能使溴水褪色,能使酸性高锰酸钾溶液褪色 |
15.X、Y、Z、W为四种短周期主族元素,原子序数依次增大.其中X、Z同主族,Y、Z同周期,Y原子的最外层电子数是次外层电子数的一半,X原子最外层电子数是核外电子层数的3倍,W的最高正价与最低负价代数和为6.下列说法正确的是( )
| A. | X、Y、Z、W四种元素的简单氢化物中,Y的气态氢化物最稳定 | |
| B. | Y、Z、W四种元素的原子半径由大到小的顺序为:Y>Z>W | |
| C. | X、Z和W三种元素形成的简单离子的半径由大到小的顺序为:W>Z>X | |
| D. | Y、Z和W三种元素的最高价氧化物对应的水化物都是强酸 |