题目内容
向含有下列离子的水溶液中,加入一小块金属钠,引起离子数目减少的是( )
| A、CO32- |
| B、OH- |
| C、HCO3- |
| D、Cu2+ |
考点:钠的化学性质,离子共存问题
专题:几种重要的金属及其化合物
分析:Na和水反应生成NaOH和氢气,OH-和HCO3-反应生成CO32-和水,据此分析解答.
解答:
解:Na和水反应生成NaOH和氢气,NaOH是强电解质,在水溶液里电离出OH-,
A.OH-和CO32-不反应,但能抑制水解,所以CO32-个数增多,故A错误;
B.NaOH是强电解质,在水溶液里电离出OH-,导致溶液中OH-个数增多,故B错误;
C.OH-和HCO3-反应生成CO32-和水,所以碳酸根离子个数减小,故C正确;
D.OH-和Cu2+反应生成氢氧化铜,所以Cu2+个数减小,故D正确;
故选C.
A.OH-和CO32-不反应,但能抑制水解,所以CO32-个数增多,故A错误;
B.NaOH是强电解质,在水溶液里电离出OH-,导致溶液中OH-个数增多,故B错误;
C.OH-和HCO3-反应生成CO32-和水,所以碳酸根离子个数减小,故C正确;
D.OH-和Cu2+反应生成氢氧化铜,所以Cu2+个数减小,故D正确;
故选C.
点评:本题考查了钠的性质及物质间的反应,明确物质的性质是解本题关键,同时考查盐类水解,题目难度不大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
下列不属于配合物的是( )
| A、[Cu(H2O)4]SO4?H2O |
| B、[Ag(NH3)2]OH |
| C、KAl(SO4)2?12H2O |
| D、Na[Al(OH)4] |
Co(Ⅲ)的八面体配合物CoClm?nNH3,若1mol配合物与AgNO3作用生成1molAgCl沉淀,则m、n的值是( )
| A、m=3 n=6 |
| B、m=3 n=4 |
| C、m=4 n=1 |
| D、m=4 n=5 |
正确表示下列反应的离子方程式的是( )
| A、氢氧化钠溶液与盐酸反应:H++OH-=H2O |
| B、铁溶于氯化铁溶液:Fe3++Fe=2Fe2+ |
| C、碳酸钙与盐酸反应:CO32-+2H+=CO2↑+H2O |
| D、钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
下列各组离子中,能在强酸性溶液里大量共存,并且溶液呈无色透明的是( )
| A、Cu2+、NO3-、Cl-、SO42- |
| B、Na+、K+、CO32-、Cl- |
| C、Mg2+、Na+、Cl-、NO3- |
| D、K+、Mg2+、ClO-、OH- |
将相同质量的铜分别与过量浓硝酸、稀硝酸在试管中反应,下列叙述正确的是( )
| A、在常温下,开始的反应速率:两者相同 |
| B、最终消耗硝酸的物质的量:前者多,后者少 |
| C、试管中气体的颜色:前者浅,后者深 |
| D、转移的电子总数:前者多,后者少 |
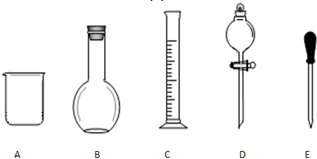 实验室需要0.1mol/L NaOH溶液480mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/L NaOH溶液480mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.