题目内容
8.下列说法正确的是( )| A. | 乙烯和苯都能使溴的四氯化碳褪色 | |
| B. | 石油分馏是物理变化,可得到汽油、煤油等物质 | |
| C. | 石油裂化主要得到乙烯 | |
| D. | 煤制煤气是物理变化,是高效、清洁地利用煤的重要途径 |
分析 A.乙烯含碳碳双键,而苯不含;
B.石油分馏得到烃类物质;
C.石油裂化主要得到汽油;
D.煤制煤气,生成CO和氢气.
解答 解:A.乙烯含碳碳双键,与溴发生加成反应使其褪色,而苯与溴的四氯化碳溶液不反应,故A错误;
B.石油分馏得到烃类物质,是物理变化,馏分中含汽油、煤油等物质,故B正确;
C.石油裂化主要得到汽油,裂解可得到乙烯,故C错误;
D.煤制煤气,生成CO和氢气,为化学变化,减少污染物的排放,是高效、清洁地利用煤的重要途径,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、石油和煤的综合应用为解答的关键,侧重分析与应用能力的考查,注意化学与生活的联系,题目难度不大.

练习册系列答案
相关题目
18.氯化硼的熔点为10.7℃,在氯化硼分子中,Cl-B-Cl键角为120℃,它可以水解,水解产物之一是硼酸(H3BO3).下列有磁氯化硼的叙述正确的是( )
| A. | 氯化硼是原子晶体 | B. | 熔化时,氯化硼能导电 | ||
| C. | 氯化硼分子是一种非极性分子 | D. | 氯化硼水解得到两种弱酸 |
19.X、Y是同周期非金属元素,已知X原子比Y原子的原子半径大,则下列叙述正确的是( )
| A. | X的最高价氧化物对应的水化物的酸性比Y的强 | |
| B. | X的阴离子比Y的阴离子的还原性强 | |
| C. | X原子的得电子能力比Y原子强 | |
| D. | X的气态氢化物比Y的气态氢化物稳定 |
16.下列有关叙述正确的是( )
| A. | 标准状况下,11.2 L苯中含有分子的数目为0.5NA | |
| B. | 制乙烯时,用排水法或向上排空气法收集气体 | |
| C. | 乙烯可作水果的催熟剂 | |
| D. | 78 g苯含有碳碳双键的数目为3NA |
3.I.有X、Y、Z、R四种短周期元素,Y、Z、R同周期.相关信息如下:
(1)Z元素在周期表的位置是第三周期第VIIA族,Y、Z、R简单离子的半径从大到小的顺序是S2->Cl->Na+(用离子符号表示);
(2)由X、Z两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子里X、Z两种原子最外层均达到8个电子的稳定结构.甲遇水蒸气可形成一种常见的漂白性物质.则甲的结构式为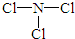 ;
;
(3)化合物乙(Y2R)溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质Y2R2,其溶液显黄色.则Y2R2的电子式为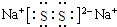 ,写出乙溶液在空气中变质过程的化学方程式4Na2S+O2+2H2O═4NaOH+2Na2S2 .
,写出乙溶液在空气中变质过程的化学方程式4Na2S+O2+2H2O═4NaOH+2Na2S2 .
II.元素X与氢可形成多种化合物,如丙、丁、戊.
(1)丙与醋酸类似,为一元弱酸,对热十分稳定但受撞击就爆炸.8.6g丙爆炸分解生成H2和6.72L(标况下)X2.写出其爆炸的化学方程式2HN3=3N2+H2 ;
(2)丁为离子化合物,遇水反应生成H2和气体戊,标况下戊的密度为0.76g•L-1,则物质丁的化学式为NH4H;
(3)戊在高温条件下能还原Fe2O3,生成两种单质,写出该反应的化学方程式2NH3+Fe2O3$\frac{\underline{\;高温\;}}{\;}$N2+2Fe+3H2O,有人提出生成的产物中可能还有FeO,请设计实验方案验证(用化学方法)取固体生成物ag与足量盐酸反应,测定生成气体标况的体积为VL,若V<$\frac{a}{56}×22.4$,则含FeO,反之则无;或者取一定质量固体生成物与足量H2(或CO)共热充分反应,若质量减少则含FeO,反之则无.
| 相关信息 | |
| X | 单质为双原子分子.若低温蒸发液态空气,因其沸点较低可先获得X的单质 |
| Y | 含Y元素的物质焰色反应为黄色 |
| Z | 同周期元素中原子半径最小 |
| R | R元素原子的最外层电子数是K层电子数的3倍 |
(2)由X、Z两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子里X、Z两种原子最外层均达到8个电子的稳定结构.甲遇水蒸气可形成一种常见的漂白性物质.则甲的结构式为
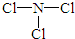 ;
;(3)化合物乙(Y2R)溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质Y2R2,其溶液显黄色.则Y2R2的电子式为
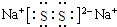 ,写出乙溶液在空气中变质过程的化学方程式4Na2S+O2+2H2O═4NaOH+2Na2S2 .
,写出乙溶液在空气中变质过程的化学方程式4Na2S+O2+2H2O═4NaOH+2Na2S2 .II.元素X与氢可形成多种化合物,如丙、丁、戊.
(1)丙与醋酸类似,为一元弱酸,对热十分稳定但受撞击就爆炸.8.6g丙爆炸分解生成H2和6.72L(标况下)X2.写出其爆炸的化学方程式2HN3=3N2+H2 ;
(2)丁为离子化合物,遇水反应生成H2和气体戊,标况下戊的密度为0.76g•L-1,则物质丁的化学式为NH4H;
(3)戊在高温条件下能还原Fe2O3,生成两种单质,写出该反应的化学方程式2NH3+Fe2O3$\frac{\underline{\;高温\;}}{\;}$N2+2Fe+3H2O,有人提出生成的产物中可能还有FeO,请设计实验方案验证(用化学方法)取固体生成物ag与足量盐酸反应,测定生成气体标况的体积为VL,若V<$\frac{a}{56}×22.4$,则含FeO,反之则无;或者取一定质量固体生成物与足量H2(或CO)共热充分反应,若质量减少则含FeO,反之则无.
20.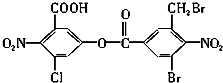 已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如下所示,1mol 该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为( )
已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如下所示,1mol 该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为( )
 已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如下所示,1mol 该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为( )
已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如下所示,1mol 该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为( )| A. | 5 mol | B. | 6 mol | C. | 7 mol | D. | 8 mol |
17.CH4分子中的4个H被苯基取代后的分子结构如图所示,则关于该有机物下列说法正确的是( )
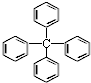

| A. | 该有机物分子式为C25H24 | |
| B. | 该多环芳烃属于稠环芳烃 | |
| C. | 该分子中最多可能有13个碳原子在同一平面上 | |
| D. | 该有机物能使酸性高锰酸钾溶液褪色 |