题目内容
11.下列说法中正确的是( )| A. | 化学反应中的能量变化都表现为热量的变化 | |
| B. | 增加炼铁高炉的高度可以降低尾气中CO的含量 | |
| C. | 吸热反应的发生都需要加热,吸热反应都没有利用价值 | |
| D. | 粉状的煤比块状的煤燃烧效率高 |
分析 A、化学反应中的能量变化可以变现为热量的变化,但不止表现为热量的变化;
B、高炉煤气成分中与高炉高度是没有关系;
C、反应吸放热与反应条件无关;
D、增大固体表面积可以增大燃烧效率.
解答 解:A、化学反应中的能量变化可以变现为热量的变化,还可以表现为光能、电能的变化等,故A错误;
B、高炉煤气成分中与高炉高度是没有关系,增加炼铁高炉的高度对尾气中CO的含量无影响,故B错误;
C、反应吸放热与反应条件无关,吸热反应不一定需要加热,吸热反应也可以有利用价值,故C错误;
D、增大固体表面积可以增大燃烧效率,故将煤粉碎能提高煤的燃烧效率,故D正确.
故选D.
点评 本题考查高炉尾气的含量,固体表面积对煤的燃烧效率的影响等问题,注意反应中的能量变化可以表现为热能、光能和电能的变化.

练习册系列答案
相关题目
2.下列叙述正确的是( )
| A. | Cl2的化学性质活泼,与H2混合后立刻发生爆炸 | |
| B. | 新制的氯水光照会产生气泡,该气体是Cl2 | |
| C. | 若发生Cl2泄露,应立即向上风地区转移 | |
| D. | 漂白粉比HClO稳定,可露置在空气中长期保存且不影响使用效果 |
19.设NA为阿伏加德罗常数,下列说法中正确的是( )
| A. | 2NA个二氧化碳分子的质量为44g | |
| B. | 2.4g金属镁与足量盐酸完全反应,失电子总数为0.2NA | |
| C. | 0.1mol/LNaCl溶液中,Na+与Cl-离子总数为0.2NA | |
| D. | 17g氨气中所含原子数为NA |
6.下列有关物质的表达式正确的是( )
| A. | 乙炔分子的比例模型示意图: | B. | 溴乙烷的电子式: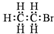 | ||
| C. | 1,3-丁二烯的分子式:C4H8 | D. | 乙醇的结构简式:CH3CH2OH |
16.下列四种固体物质中,既存在离子键又存在共价键的是( )
| A. | NH4Cl | B. | K2S | C. | MgCl2 | D. | SO3 |
3.将钠、镁、铝各0.3mol 分别放入100mL1mol/L 的盐酸中,同温同压下产生的气体体积比是( )
| A. | 1:1:1 | B. | 3:1:1 | C. | 1:2:3 | D. | 6:3:2 |
20.元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )
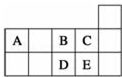

| A. | D在过量的B中燃烧的主要产物为DB3 | |
| B. | C的氢化物的水溶液酸性比E的强 | |
| C. | D与B形成的阴离子可能有DB32-、DB42- | |
| D. | E单质由于分子间形成了氢键,所以很容易液化 |
1.在溶液中能大量共存,若加入OH-有沉淀析出,若加入H+能放出气体的是( )
| A. | Mg2+、Na+、Cl-、CO${\;}_{3}^{2-}$ | B. | Ba2+、K+、NO${\;}_{3}^{-}$、Cl- | ||
| C. | Fe3+、NH${\;}_{4}^{+}$、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ | D. | Na+、Ca2+、Cl-、HCO${\;}_{3}^{-}$ |