题目内容
1.在溶液中能大量共存,若加入OH-有沉淀析出,若加入H+能放出气体的是( )| A. | Mg2+、Na+、Cl-、CO${\;}_{3}^{2-}$ | B. | Ba2+、K+、NO${\;}_{3}^{-}$、Cl- | ||
| C. | Fe3+、NH${\;}_{4}^{+}$、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ | D. | Na+、Ca2+、Cl-、HCO${\;}_{3}^{-}$ |
分析 A.镁离子与碳酸根离子反应生成碳酸镁沉淀;
B.四种离子之间能够共存,但是加入氢氧根离子无沉淀,加入氢离子无气体产生;
C.四种离子之间不反应,但是加入桥梁不会生成气体;
D.四种离子之间能够共存,钙离子、碳酸氢根离子与氢氧根离子生成碳酸钙沉淀,碳酸氢根离子与氢离子反应生成二氧化碳气体.
解答 解:A.Mg2+、CO32-结合生成沉淀,不能大量共存,故A错误;
B.Ba2+、K+、Cl-、NO3-之间不反应,能够大量共存,但是加入OH-无沉淀析出,加入H+无气体放出,故B错误;
C.Fe3+、NH4+、SO42-、NO3-之间不反应,加入OH-有氢氧化铁沉淀析出,但是加入H+没有气体放出,故C错误;
D.Na+、Ca2+、Cl-、HCO3-之间不发生反应,能够共存,若加入OH-有碳酸钙沉淀析出,若加入H+能放出二氧化碳气体,满足条件,故D正确;
故选D.
点评 本题考查离子的共存问题,题目难度不大,明确离子之间的反应及复分解反应发生的条件即可解答,注意掌握离子共存的条件,还要明确题干暗含条件的含义,试题侧重考查学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
相关题目
11.下列说法中正确的是( )
| A. | 化学反应中的能量变化都表现为热量的变化 | |
| B. | 增加炼铁高炉的高度可以降低尾气中CO的含量 | |
| C. | 吸热反应的发生都需要加热,吸热反应都没有利用价值 | |
| D. | 粉状的煤比块状的煤燃烧效率高 |
12.检验酒精中是否含有少量水,可选用的试剂是( )
| A. | 生石灰 | B. | 金属钠 | C. | 浓硫酸 | D. | 无水硫酸铜 |
9.下列反应属于有机物被还原的是( )
| A. | 乙醛发生银镜反应 | B. | 新制Cu(OH)2与乙醛反应 | ||
| C. | 乙醛加氢制乙醇 | D. | 乙醛制乙酸 |
16.下列说法正确的是 ( )
| A. | 在浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 | |
| B. | 葡萄糖注射液不产生丁达尔效应,不属于胶体 | |
| C. | 在Fe(0H)3胶体中.H+、K+、S2-、Br-能大量共存 | |
| D. | 明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 |
6.下列说法正确的是 ( )
| A. | 元素的非金属性越强,其对应的简单氢化物的水溶液酸性越强 | |
| B. | 用pH试纸测定NaC1O液的pH值大于7 | |
| C. | 酸性气体不一定都能用浓硫酸干燥 | |
| D. | SO2和SO3混合气体通入Ba(NO3)2溶液可得到BaSO3和BaSO4 |
3.下列有机物命名正确的是( )
| A. |  2-乙基丙烷 2-乙基丙烷 | B. |  间二甲苯 间二甲苯 | ||
| C. | CH3CH2CH2CH2OH 1-丁醇 | D. | 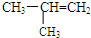 2-甲基-2-丙烯 2-甲基-2-丙烯 |
20.胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统.实验测得101kPa时,1mol H2完全燃烧生成液态水,放出285.8kJ的热量;1mol CH3OH(l)完全燃烧生成液态水和CO2,放出725.76kJ的热量.下列热化学方程式书写正确的是( )
| A. | CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=+725.76 kJ•mol-1 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ•mol-1 | |
| C. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-1451.52 kJ•mol-1 | |
| D. | 稀HCl与氨水反应生成1 mol H2O所放出的热量为中和热 |
1.下列物质中,既能与强酸又能与强碱反应的是( )
①(NH4)2CO3 ②NaHCO3 ③Al2O3 ④Al(OH)3.
①(NH4)2CO3 ②NaHCO3 ③Al2O3 ④Al(OH)3.
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ②③④ |