题目内容
17.下列各组离子一定能大量共存的是( )| A. | 在无色溶液中:NH4+、Fe2+、SO42-、CO32- | |
| B. | 在含有大量Ba2+ 的溶液中:NH4+、Na+、Cl-、CO32- | |
| C. | 在强碱性溶液中:Na+、Cl-、K+、SO42- | |
| D. | 在强酸性溶液中:K+、Fe2+、Cl-、HCO3- |
分析 A.Fe2+为浅绿色;
B.离子之间结合生成沉淀;
C.强碱溶液中该组离子之间不反应;
D.强酸溶液中含大量的氢离子.
解答 解:A.Fe2+为浅绿色,与无色不符,且Fe2+、CO32-结合生成沉淀,不能大量共存,故A错误;
B.Ba2+、CO32-结合生成沉淀,不能大量共存,故B错误;
C.强碱溶液中该组离子之间不反应,可大量共存,故C正确;
D.强酸溶液中含大量的氢离子,H+、HCO3-结合生成水和气体,不能大量共存,故D错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
7.用如图装置不能达到有关实验目的是( ) 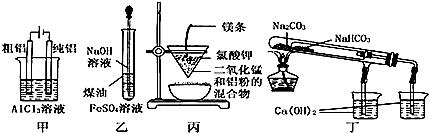

| A. | 用甲图装置电解精炼铝 | |
| B. | 用乙图装置制备 Fe(OH)2 | |
| C. | 用丙图装置可制得金属锰 | |
| D. | 用丁图装置验证 NaHCO3 和 Na2CO3的热稳定性 |
2.如图为海水综合利用的工业流程图,判断下列说法正确的是( )

| A. | 过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 | |
| B. | 在过程③中将MgCl2•6H2O灼烧即可制得无水MgCl2 | |
| C. | 在过程④、⑥反应中每氧化0.2 mol Br-需消耗0.1mol Cl2 | |
| D. | 除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
9.对下列物质分类全部正确的是( )
①食盐水
②NaOH
③盐酸
④液态氧
⑤蔗糖
⑥KClO3.
①食盐水
②NaOH
③盐酸
④液态氧
⑤蔗糖
⑥KClO3.
| A. | 纯净物②③⑥ | B. | 混合物①③④ | C. | 电解质②⑥ | D. | 非电解质④⑤ |
18.某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.
(1)根据表中数据,在图1中相应位置上画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
(2)该反应达到平衡时反应物X的转化率α等于45%;

(3)如果该反应是放热反应.改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如图2所示),则曲线①、②、③改变的实验条件分别是:
①升高温度;
②使用催化剂;
③增大压强.
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
(2)该反应达到平衡时反应物X的转化率α等于45%;

(3)如果该反应是放热反应.改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如图2所示),则曲线①、②、③改变的实验条件分别是:
①升高温度;
②使用催化剂;
③增大压强.


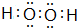 该物质能使酸性KMnO4溶液褪色,在这个反应中体现了该物质的还原性(填“氧化性”或“还原性”)
该物质能使酸性KMnO4溶液褪色,在这个反应中体现了该物质的还原性(填“氧化性”或“还原性”)