题目内容
9.对下列物质分类全部正确的是( )①食盐水
②NaOH
③盐酸
④液态氧
⑤蔗糖
⑥KClO3.
| A. | 纯净物②③⑥ | B. | 混合物①③④ | C. | 电解质②⑥ | D. | 非电解质④⑤ |
分析 纯净物是指由一种物质组成的物质.混合物是两种或两种以上的物质组成.水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质;在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;单质,混合物既不是电解质也不是非电解质.
解答 解:①食盐水含有氯化钠和水,属于混合物;
②NaOH为碱,水溶液中或熔融状态下能够导电,属于电解质;
③盐酸含有氯化氢和水,属于混合物;
④液态氧属于单质,既不是电解质也不是非电解质;
⑤蔗糖水溶液中和熔融状态下都不能够导电,属于非电解质;
⑥KClO3为盐,水溶液中或熔融状态下能够导电,属于电解质;
综上只有C正确,
故选C.
点评 本题主要考查纯净物、混合物、电解质、非电解质的定义,注意对概念的理解和区分,正确从宏观组成和微观构成两个角度来把握,题目较简单.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案
相关题目
20.下列有关化学反应速率的说法正确的是( )
| A. | 用铁片和稀硫酸反应制氢气时,可改用98%的浓硫酸加快生成氢气速率 | |
| B. | 100 mL 2 mol•L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 | |
| C. | 汽车尾气中NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢 | |
| D. | SO2的催化氧化是一个放热反应,所以升高温度,反应速率减慢 |
17.下列各组离子一定能大量共存的是( )
| A. | 在无色溶液中:NH4+、Fe2+、SO42-、CO32- | |
| B. | 在含有大量Ba2+ 的溶液中:NH4+、Na+、Cl-、CO32- | |
| C. | 在强碱性溶液中:Na+、Cl-、K+、SO42- | |
| D. | 在强酸性溶液中:K+、Fe2+、Cl-、HCO3- |
4. 乙酰苯胺是常用的医药中间体,可由苯胺与乙酸制备.反应的化学方程式如下:
乙酰苯胺是常用的医药中间体,可由苯胺与乙酸制备.反应的化学方程式如下:
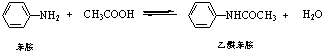
有关化合物的物理性质见下表:
合成:
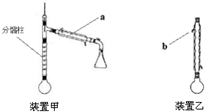
方案甲:采用装置甲(分馏柱的作用类似于石油分馏中的分馏塔).在圆底烧瓶中加入5,0mL 苯胺、7.4mL乙酸,加热至沸,控制温度计读数100~105℃,保持液体平缓流出,反应40min后停止加热.将圆底烧瓶中的液体趁热倒入盛有100mL水的烧杯,冷却后有乙酰苯胺固体析出,过滤得粗产物.
方案乙:采用装置乙,加热回流,反应40min后停止加热.其余与方案甲相同.
提纯:甲乙两方案均采用重结晶方法.操作如下:
①加热溶解→②活性炭脱色→③趁热过滤→④冷却结晶→⑤过滤→⑥洗涤→⑦干燥
请回答:
(1)仪器a的名称是冷凝管,b处水流方向是出水(填“进水”或“出水”).
(2)合成步骤中,乙酰苯胺固体析出后,过滤分离出粗产物.留在滤液中的主要物质是乙酸.
(3)提纯过程中的第③步,过滤要趁热的理由是防止温度降低导致乙酰苯胺析出,降低产率.
(4)提纯过程第⑥步洗涤,下列洗涤剂中最合适的是A.
A.蒸馏水 B.乙醇 C.5%Na2CO3溶液 D.饱和NaCl溶液
(5)从投料量分析,为提高乙酰苯胺产率,甲乙两种方案均采取的措施是乙酸过量;实验结果表明方案甲的产率较高,原因是方案甲将反应过程中生成的水蒸出,促进反应.
 乙酰苯胺是常用的医药中间体,可由苯胺与乙酸制备.反应的化学方程式如下:
乙酰苯胺是常用的医药中间体,可由苯胺与乙酸制备.反应的化学方程式如下: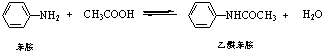
有关化合物的物理性质见下表:
| 化合物 | 密度(g.cm-3) | 溶解性 | 熔点(℃) | 沸点(℃) |
| 乙酸 | 1.05 | 易溶于水、乙醇 | 17 | 118 |
| 苯胺 | 1.02 | 微溶于水,易溶于乙醇 | -6 | 184 |
| 乙酰苯胺 | - | 微溶于冷水,可溶于热水,易溶于乙醇 | 114 | 304 |
方案甲:采用装置甲(分馏柱的作用类似于石油分馏中的分馏塔).在圆底烧瓶中加入5,0mL 苯胺、7.4mL乙酸,加热至沸,控制温度计读数100~105℃,保持液体平缓流出,反应40min后停止加热.将圆底烧瓶中的液体趁热倒入盛有100mL水的烧杯,冷却后有乙酰苯胺固体析出,过滤得粗产物.
方案乙:采用装置乙,加热回流,反应40min后停止加热.其余与方案甲相同.
提纯:甲乙两方案均采用重结晶方法.操作如下:
①加热溶解→②活性炭脱色→③趁热过滤→④冷却结晶→⑤过滤→⑥洗涤→⑦干燥
请回答:
(1)仪器a的名称是冷凝管,b处水流方向是出水(填“进水”或“出水”).
(2)合成步骤中,乙酰苯胺固体析出后,过滤分离出粗产物.留在滤液中的主要物质是乙酸.
(3)提纯过程中的第③步,过滤要趁热的理由是防止温度降低导致乙酰苯胺析出,降低产率.
(4)提纯过程第⑥步洗涤,下列洗涤剂中最合适的是A.
A.蒸馏水 B.乙醇 C.5%Na2CO3溶液 D.饱和NaCl溶液
(5)从投料量分析,为提高乙酰苯胺产率,甲乙两种方案均采取的措施是乙酸过量;实验结果表明方案甲的产率较高,原因是方案甲将反应过程中生成的水蒸出,促进反应.
14.下列说法中正确的是( )
| A. | 25℃时,NH4Cl和NH3.H2O的混合液中离子浓度可能为C(NH4+)>C(Cl-)>C(OH-)>C(H+) | |
| B. | 向0.1mol/L的CuSO4溶液中加入少量蒸馏水,溶液酸性减弱,Cu2+水解程度降低 | |
| C. | 25℃时,PH=12的NaOH溶液、PH=12的CH3COONa溶液、PH=2的硫酸,三种溶液中水的电离程度相同 | |
| D. | 25℃时,向稀氨水中通入NH3,溶液中C(OH-)减小 |
18.下列有关工业冶炼镁的说法不正确的是( )
| A. | 从节能角度考虑,工业选择无水氯化镁为原料冶炼镁,不选择氧化镁 | |
| B. | 若电解熔融氯化镁时有少量水,镁可能与水蒸气反应 | |
| C. | 阳极可以用不活泼金属铜、银 | |
| D. | 用湿润的KI淀粉试纸可以检阳极产生的气体 |
10.下列说法正确的是( )
| 选项 | 实验 | 解释或结论 |
| A | 用洁净的Pt丝蘸取某溶液进行焰色反应,火焰呈黄色 | 该溶液中一定不含有K+ |
| B | 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧 | CO2、H2O与Na2O2反应是放热反应 |
| C | 向某溶液中滴加硝酸酸化的Ba(NO3)2溶液产生白色沉淀 | 该溶液中含有SO42- |
| D | 利用一束强光照射明矾溶液,产生光亮的“通路”, | 明矾一定发生了水解 |
| A. | A | B. | B | C. | C | D. | D |
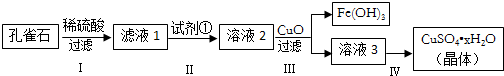
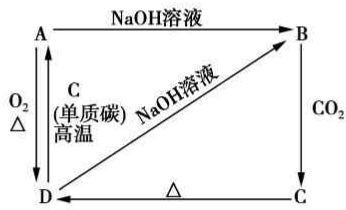 已知A是灰黑色、有金属光泽的固体单质.根据如图所示的物质之间的转化关系,回答下列有关问题. (1)写出B、C两物质的名称:B硅酸钠,C硅酸.
已知A是灰黑色、有金属光泽的固体单质.根据如图所示的物质之间的转化关系,回答下列有关问题. (1)写出B、C两物质的名称:B硅酸钠,C硅酸.