题目内容
17.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 加入KSCN溶液变红色的溶液:NH4+、K+、I-、SO42- | |
| B. | 在pH=11的溶液中:Na+、AlO2-、NO3-、S2-、SO32- | |
| C. | 由水电离的c(OH-)=10-13mol•L-1的溶液中:Na+、Cl-、HCO3-、NO3- | |
| D. | 使甲基橙变红色的溶液:Fe2+、K+、SO42-、NO3- |
分析 A.加入KSCN溶液变红色的溶液,含铁离子;
B.在pH=11的溶液,溶液显碱性;
C.由水电离的c(OH-)=10-13mol•L-1的溶液,为酸或碱溶液;
D.使甲基橙变红色的溶液,显酸性,离子之间发生氧化还原反应.
解答 解:A.加入KSCN溶液变红色的溶液,含铁离子,与I-发生氧化还原反应,不能大量共存,故A错误;
B.在pH=11的溶液,溶液显碱性,该组离子之间不反应,可大量共存,故B正确;
C.由水电离的c(OH-)=10-13mol•L-1的溶液,为酸或碱溶液,HCO3-与酸、碱均反应,一定不能大量共存,故C错误;
D.使甲基橙变红色的溶液,显酸性,Fe2+、H+、NO3-发生氧化还原反应.不能大量共存,故D错误;
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重氧化还原反应、复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
8.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 2.4g金属镁所含电子数目为1.2NA | B. | 16g CH4所含原子数目为NA | ||
| C. | 17gNH3所含中子数目为10 NA | D. | 18g水所含分子数目为NA |
5.下列离子方程式书写正确的是( )
| A. | 铁与稀硫酸反应 Fe+2H+═Fe3++H2↑ | |
| B. | 氢氧化铝与足量盐酸反应 Al(OH)3+3H+═Al3++3H2O | |
| C. | 钠和冷水反应 Na+2H2O═Na++H2↑+OH- | |
| D. | 铜片与稀硝酸反应 Cu+NO3-+4H+═Cu2++NO↑+2H2O |
2.五种固体物质A、B、C、D、E由下表中不同的阴阳离子组成,它们均易溶于水.
分别取它们的水溶液进行实验,结果如下:
①A溶液与C溶液混合后产生蓝色沉淀,向该沉淀中加入足量稀HNO3,沉淀部分溶解,剩余白色固体;
②B溶液与E溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④B溶液与D溶液混合后无现象;
⑤将38.4g Cu片投入装有足量D溶液的试管中,Cu片不溶解,再滴加500mL1.6mol•L-1稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.
(1)据此推断A、D的化学式为:ACuSO4;DAl(NO3)3.
(2)写出步骤①中生成沉淀的反应的离子方程式Cu2++SO42-+Ba2++2OH-=Cu(OH)2↓+BaSO4↓.
(3若向E的饱和溶液中通入足量的CO2,现象是溶液由澄清变浑浊,原因是Na2CO3+CO2+H2O=2NaHCO3↓,由于NaHCO3的溶解度小于Na2CO3溶解度,并且溶质的质量增加同时溶剂的质量减少,因此会有晶体析出而变浑浊(用化学方程式及必要的文字说明解释).
(4)步骤⑤中产生的有害气体可用NaOH溶液吸收.
| 阳离子 | Na+ Al3+Fe3+ Cu2+、Ba2+ |
| 阴离子 | OH- Cl- CO32- NO3- SO4- |
①A溶液与C溶液混合后产生蓝色沉淀,向该沉淀中加入足量稀HNO3,沉淀部分溶解,剩余白色固体;
②B溶液与E溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④B溶液与D溶液混合后无现象;
⑤将38.4g Cu片投入装有足量D溶液的试管中,Cu片不溶解,再滴加500mL1.6mol•L-1稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.
(1)据此推断A、D的化学式为:ACuSO4;DAl(NO3)3.
(2)写出步骤①中生成沉淀的反应的离子方程式Cu2++SO42-+Ba2++2OH-=Cu(OH)2↓+BaSO4↓.
(3若向E的饱和溶液中通入足量的CO2,现象是溶液由澄清变浑浊,原因是Na2CO3+CO2+H2O=2NaHCO3↓,由于NaHCO3的溶解度小于Na2CO3溶解度,并且溶质的质量增加同时溶剂的质量减少,因此会有晶体析出而变浑浊(用化学方程式及必要的文字说明解释).
(4)步骤⑤中产生的有害气体可用NaOH溶液吸收.

 Ⅰ.在某温度时按n(N2):n(H2)=1:3的比例将混合气体投入密闭容器中反应:N2(g)+3H2(g)═2NH3(g)△H<0;
Ⅰ.在某温度时按n(N2):n(H2)=1:3的比例将混合气体投入密闭容器中反应:N2(g)+3H2(g)═2NH3(g)△H<0;

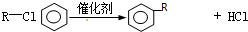
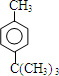 ;E
;E .
. .
. .
.