题目内容
13.下列物质中,能发生水解反应,但不能发生消去反应的是( )| A. | CH3CH2CH2CH2Cl | B. | CH3CH2Cl | C. | CH3Br | D. |  |
分析 由选项可知,均为卤代烃,均可发生水解反应,与-X相连C的邻位C上有H可发生消去反应,以此来解答.
解答 解:A.CH3CH2CH2CH2Cl可水解CH3CH2CH2CH2OH,发生消去反应生成CH3CH2CH=CH2,故A不选;
B.CH3CH2Cl可发生水解反应生成CH3CH2OH,发生消去反应生成CH2=CH2,故B不选;
C.CH3Br没有邻位C,不能发生消去反应,CH3Br水解生成CH3OH,故C选;
D. 没有邻位C,不能发生消去反应,可发生水解反应生成醇,故D选;
没有邻位C,不能发生消去反应,可发生水解反应生成醇,故D选;
故选CD.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,把握有机物的官能团的性质为解答该题的关键,题目难度不大,注意卤代烃消去反应的结构特点.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
1.烃的含碳量随碳原子数的增加呈现的一定的递变规律,关于下图的说法错误的是( )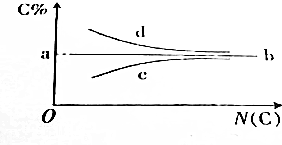

| A. | a点的值肯定是85.7% | B. | 满足b线走势的烃通式为CnH2n | ||
| C. | 满足c线走势的烃一定是烷烃 | D. | 满足d线走势的烃一定是炔烃 |
 酚
酚 羧酸
羧酸 醛
醛 卤代烃
卤代烃 酯.
酯. )具有多种同分异构体.
)具有多种同分异构体. ;②
;② ;③
;③ ;
;