题目内容
18.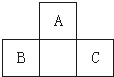 A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组元素是( )
A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组元素是( )| A. | Be、Na、Al | B. | B、Mg、Si | C. | C、Al、P | D. | O、P、Cl |
分析 由短周期元素A、B、C在周期表中的位置,可知A处于第二周期,B、C处于第三周期,令A的原子序数为x,用x表示出B、C的原子序数,根据B、C元素的原子序数之和是A元素原子序数的4倍列方程求x,判断A、B、C元素.
解答 解:令A的原子序数为x,则B的原子序数为x+8-1,C的原子序数为x+8+1,则:(x+8-1)+(x+8+1)=4x,解得x=8,所以A为O元素,B为P元素,C为Cl元素,
故选:D.
点评 本题考查元素周期表的结构,难度不大,根据短周期特点确定元素所在周期,注意掌握同主族元素原子序数关系,利用最外层电子数确定更简单.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
8.1905年德国化学家哈伯发明了合成氨的方法,他因此获得了1918年度诺贝尔化学奖.哈伯法合成氨需要20-50Mpa的高压和500℃的高温下,用铁作催化剂,且氨的产率为10%-15%.2005年美国俄勒冈大学的化学家使用了一种名为transFe(DMeOPrPE)2C12的铁化合物作催化剂,在常温常压下合成出氨,反应可表示为N2+3H2=2NH3,下列有关说法正确的是( )
| A. | 不同的催化剂对化学反应速率的影响均相同 | |
| B. | 哈伯法合成氨是吸热反应,新法合成氨是放热反应 | |
| C. | 新法合成能在常温下进行是因为不需要锻炼化学键 | |
| D. | 新法合成与哈伯法相比不需要在高温条件下,可节约大量能源,极具发展愿景 |
9.对于反应N2+O2?2NO在密闭容器中进行,下列哪些条件能加快该反应的化学反应速率( )
| A. | 体积不变充入N2使压强增大 | B. | 体积不变充入O2使压强增大 | ||
| C. | 使体积增大到原来的2倍 | D. | 体积不变充入氦气使压强增大 |
6.如表中实验操作能达到实验目的是( )
| 选项 | 实验操作 | 实验目的 |
| A | 向甲酸钠溶液中加新制的Cu(OH)2并加热 | 确定甲酸钠具有醛基性质 |
| B | 加溴水,振荡,过滤除去沉淀 | 除去苯中混有的苯酚 |
| C | 向酒精和水的混合溶液中加入金属钠 | 确定酒精中混有水 |
| D | 将氯乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验水解产物中的氯离子 |
| A. | A | B. | B | C. | C | D. | D |
13.在一定条件下,按下列物质的量关系进行反应,其对应的离子方程式或化学方程式书写正确的是( )
| A. | n(Cl2):n(Fe)=5:4 5Cl2+4Fe$\frac{\underline{\;点燃\;}}{\;}$2FeCl2+2FeCl3 | |
| B. | n(Cl2):n(FeBr2)=1:1 Fe2++2Br-+Cl2=Fe3++Br2+2Cl- | |
| C. | n(MnO4-):n(H2O2)=2:3 2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O | |
| D. | n(Fe):n[HNO3(稀)]=1:3 4Fe+12H++3NO3-═3Fe2++Fe3++3NO↑+6H2O |
3.将2.3gNa放入97.8g水中,不可能出现的现象是( )
| A. | 钠熔成光亮小球 | B. | 钠浮在水面上 | ||
| C. | 有气泡产生 | D. | 溶液质量分数为4.0% |
7.下列方程式书写正确的是( )
| A. | NH4Cl的水解方程式:NH4++H2O═NH3•H2O+H+ | |
| B. | NH3•H2O的电离方程式:NH3•H2O?NH4++OH- | |
| C. | CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- | |
| D. | HCO3-的电离方程式:HCO3-+H2O?H2CO3+OH- |
