题目内容
1.利用液化石油气中的丙烷脱氢可制取丙烯:C3H8(g)?C3H6(g)+H2(g)△H.起始时,向一密闭容器中充入一定量的丙烷,在不同温度、压强下测得平衡时反应体系中丙烷与丙烯的物质的量分数如图所示(已知p1为0.1MPa).
(1)反应的△H>(填“>”“<”或“=”)0,压强p2<0.1MPa.
(2)图中A点丙烷的转化率为50%.
(3)若图中A、B两点对应的平衡常数用K(A)、K(B)表示,则K(A)<(填“>”“<”或“=”)K(B)
分析 (1)图象中物质的量分数随温度升高丙烯增加,丙烷减少,说明升温平衡正向进行;温度一定,压强越大平衡逆向进行,结合化学平衡移动原理分析压强大小;
(2)图中A点丙烷的物质的量分数为33.3%为$\frac{1}{3}$,结合化学平衡三行计算得到;
(3)若图中A、B两点对应的平衡常数用K(A)、K(B)表示,反应为吸热反应升温平衡正向进行,平衡常数增大;
解答 解:(1)图象中物质的量分数随温度升高丙烯增加,丙烷减少,说明升温平衡正向进行,正反应为吸热反应,反应的△H<0,温度一定,压强越大平衡逆向进行,P2压强下丙烯物质的量分数大于P1状态,说明P2<P1,平衡正向进行,
故答案为:>;<;
(2)图中A点丙烷的物质的量分数为33.3%为$\frac{1}{3}$,设丙烷起始量为x,消耗量为y,结合化学三行计算列式,
C3H8(g)?C3H6(g)+H2(g)
起始量(mol) x 0 0
变化量(mol) y y y
A点量(mol)x-y y y
$\frac{x-y}{x+y}$=$\frac{1}{3}$,
丙烷的转化率=$\frac{y}{x}$×100%=50%,
故答案为:50%;
(3)若图中A、B两点对应的平衡常数用K(A)、K(B)表示,反应为吸热反应升温平衡正向进行,平衡常数增大,A点温度低于B点温度,则平衡常数K(A)<K(B),
故答案为:<;
点评 本题考查了化学平衡影响因素、化学平衡转化率计算,平衡常数影响因素分析判断等知识点,掌握基础是解题关键,题目难度中等.

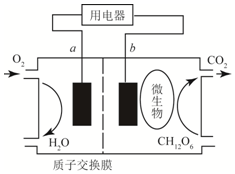
| A. | 该电池能够将电能转化为化学能 | |
| B. | b为该电池的正极 | |
| C. | 放电过程中,H+从a极区向b极区迁移 | |
| D. | 在电池反应中,正极上每消耗5.6L(标准状况下)气体时,则有NA个H通过质子交换膜 |
| I/kJ•mol-1 | I1 | I2 | I3 | I4 |
| X | 738 | 1451 | 7733 | 10540 |
| Y | 496 | 4562 | 6912 | 9540 |
| Z | 577 | 1817 | 2745 | 11578 |
| A. | c(Na+):①>②>③ | B. | 水电离的c(OH-):③>②>① | ||
| C. | 离子总浓度:③>②>① | D. | pH:①>②>③ |
| A. | 乙醚和乙醇互为同分异构体 | |
| B. | 糖类、油脂、蛋白质均能发生水解反应 | |
| C. | 聚氯乙烯可用作生产食品包装材料的原料 | |
| D. | 分子式为C3H8O的有机物,只有2种能发生酯化反应 |