题目内容
1mol某有机物A具有下列化学性质:
①与足量Na反应生成1mol H2;
②与足量碳酸氢钠反应放出1mol CO2气体;
③其蒸气对氢气的相对密度为38;
④2摩尔的A发生分子间酯化反应生成一种六元环的化合物B和2mol H2O.
(1)该有机物结构简式为 .
(2)写出A与NaOH溶液反应的化学方程式 .
(3)B的结构简式为 .
①与足量Na反应生成1mol H2;
②与足量碳酸氢钠反应放出1mol CO2气体;
③其蒸气对氢气的相对密度为38;
④2摩尔的A发生分子间酯化反应生成一种六元环的化合物B和2mol H2O.
(1)该有机物结构简式为
(2)写出A与NaOH溶液反应的化学方程式
(3)B的结构简式为
考点:有机物实验式和分子式的确定
专题:有机化学基础
分析:(1)1mol某有机物A具有下列化学性质:
①与足量Na反应生成1mol H2;说明含羟基或羧基;
②与足量碳酸氢钠反应放出1mol CO2气体;说明分子中含1个羧基和1个羧基;
③其蒸气对氢气的相对密度为38;可计算出A的相对分子质量为:38×2=76,76-17-45=14,分子中含1个CH2,综上可写出A的结构简式;
(2)羧基具有酸性,和碱发生中和反应;
(3)2摩尔的A发生分子间酯化反应生成一种六元环的化合物B和2mol H2O,根据酯化反应规律写出B的结构简式.
①与足量Na反应生成1mol H2;说明含羟基或羧基;
②与足量碳酸氢钠反应放出1mol CO2气体;说明分子中含1个羧基和1个羧基;
③其蒸气对氢气的相对密度为38;可计算出A的相对分子质量为:38×2=76,76-17-45=14,分子中含1个CH2,综上可写出A的结构简式;
(2)羧基具有酸性,和碱发生中和反应;
(3)2摩尔的A发生分子间酯化反应生成一种六元环的化合物B和2mol H2O,根据酯化反应规律写出B的结构简式.
解答:
解:(1)1mol某有机物A具有下列化学性质:
①与足量Na反应生成1mol H2;说明含羟基或羧基;
②与足量碳酸氢钠反应放出1mol CO2气体;说明分子中含1个羧基和1个羧基;
③其蒸气对氢气的相对密度为38;可计算出A的相对分子质量为:38×2=76,76-17-45=14,分子中含1个CH2,综上可写出A的结构简式为:CH2OHC00H;
故答案为:CH2OHC00H;
(2)CH2OHC00H具有酸性,和碱发生中和反应,反应方程式为:CH2OHC00H+NaOH→CH2OHC00Na+H2O;
故答案为:CH2OHC00H+NaOH→CH2OHC00Na+H2O;
(3)2摩尔的A发生分子间酯化反应生成一种六元环的化合物B和2mol H2O,根据酯化反应规律写出B的结构简式为: ;
;
故答案为 .
.
①与足量Na反应生成1mol H2;说明含羟基或羧基;
②与足量碳酸氢钠反应放出1mol CO2气体;说明分子中含1个羧基和1个羧基;
③其蒸气对氢气的相对密度为38;可计算出A的相对分子质量为:38×2=76,76-17-45=14,分子中含1个CH2,综上可写出A的结构简式为:CH2OHC00H;
故答案为:CH2OHC00H;
(2)CH2OHC00H具有酸性,和碱发生中和反应,反应方程式为:CH2OHC00H+NaOH→CH2OHC00Na+H2O;
故答案为:CH2OHC00H+NaOH→CH2OHC00Na+H2O;
(3)2摩尔的A发生分子间酯化反应生成一种六元环的化合物B和2mol H2O,根据酯化反应规律写出B的结构简式为:
 ;
;故答案为
 .
.
点评:本题考查了有机物结构式的确定和性质,中等难度,根据性质推出结构,利用所含官能团判断性质,注意官能团所代表的性质.

练习册系列答案
相关题目
下列有关铝化合物说法正确的是( )
| A、氧化铝的熔点很高,所以不可以用来冶炼铝 |
| B、氢氧化铝可以和悬浮于水中的泥沙形成絮状不溶物沉降下来,使水澄清,所以明矾可用作净水剂 |
| C、实验室可以用过量氢氧化钠与氯化铝来制备氢氧化铝 |
| D、氢氧化铝既可与酸反应又可与碱反应,是两性氢氧化物 |
明矾可以净水是因为( )
| A、明矾在水中能电离出SO42- |
| B、明矾中含有多种阳离子 |
| C、明矾溶于水后可以生成Al(OH)3胶体 |
| D、明矾可以与碱反应生成Al(OH)3沉淀 |
下列仪器常用于物质分离的是( )
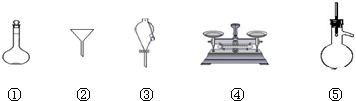

| A、①④⑤ | B、②④⑤ |
| C、②③⑤ | D、①③⑤ |
 将X气体(或溶液)慢慢通入(或加人)一定量的Y溶液中,产生沉淀量与加入X的物质的量(mol)的关系如图所示,符合如图情况的是( )
将X气体(或溶液)慢慢通入(或加人)一定量的Y溶液中,产生沉淀量与加入X的物质的量(mol)的关系如图所示,符合如图情况的是( )| A、X为NaOH溶液,Y为AlCl3溶液 |
| B、X为CO2,Y为Ca(OH)2溶液 |
| C、X为NH3,Y为AlCl3溶液 |
| D、X为HCl溶液,Y为Na[Al(OH)4]溶液 |
化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A、明矾水解生成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| B、高温电解Al2O3可制得金属铝 |
| C、MgO的熔点很高,可用于制作耐高温材料 |
| D、根据冷的浓硫酸可以用铝质容器储存的事实,说明常温下铝不会与浓硫酸发生反应 |
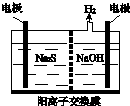 Ⅰ硫化氢的转化是资源利用和环境保护的重要研究课题.由硫化氢获得硫单质有多种方法.
Ⅰ硫化氢的转化是资源利用和环境保护的重要研究课题.由硫化氢获得硫单质有多种方法.