题目内容
在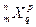 中,m、n、p、q表示某元素的四个角码。若x1与x2的q均为1,m、p对应相等,n不相等,则x1、x2表示的可能是( )
中,m、n、p、q表示某元素的四个角码。若x1与x2的q均为1,m、p对应相等,n不相等,则x1、x2表示的可能是( )
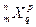 中,m、n、p、q表示某元素的四个角码。若x1与x2的q均为1,m、p对应相等,n不相等,则x1、x2表示的可能是( )
中,m、n、p、q表示某元素的四个角码。若x1与x2的q均为1,m、p对应相等,n不相等,则x1、x2表示的可能是( )| A.不同的原子 |
| B.不同的元素 |
| C.同种元素的不同原子形成的离子 |
| D.不同元素的离子 |
AC
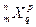 中四个角码的含义:n为质量数,m为质子数,p为离子的电荷数,q为原子个数;q均为1,则X1、X2为原子或单核离子;m相等,X1、X2为同种元素的原子或单核离子;n不相等,X1、X2为同种元素的不同原子或单核离子;若p=0,X1、X2为同种元素的不同原子,若p相等且不等于0,X1、X2为同种元素的不同原子形成的离子。
中四个角码的含义:n为质量数,m为质子数,p为离子的电荷数,q为原子个数;q均为1,则X1、X2为原子或单核离子;m相等,X1、X2为同种元素的原子或单核离子;n不相等,X1、X2为同种元素的不同原子或单核离子;若p=0,X1、X2为同种元素的不同原子,若p相等且不等于0,X1、X2为同种元素的不同原子形成的离子。
练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
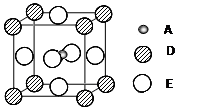
 请回答下列问题:
请回答下列问题: