题目内容
在等物质的量的短周期金属A和B中,分别加入足量的酸,A中加入盐酸,在B中加入稀硫酸,反应完全后,生成氢气的体积分别为V(A)和V(B),而且V(A)≠V(B)。若要确定反应生成物A和B的化合价,至少还需要知道的数据是( )
A.V(A)∶V(B)的值
B.V(A)或V(B)的值
C.A(或B)的物质的量
D.盐酸或硫酸的物质的量浓度
A.V(A)∶V(B)的值
B.V(A)或V(B)的值
C.A(或B)的物质的量
D.盐酸或硫酸的物质的量浓度
A
题目涉及了一定的知识面,包括元素周期表、金属与酸的反应、物质的量以及化合价等,均为我们较熟悉的知识。在元素周期表中,短周期元素的金属单质都处于金属活动顺序表内氢以前,因而它们与盐酸、稀硫酸都可以发生置换反应。由于所用的酸都是过量的,因此用什么酸以及所用的酸的浓度是多少无关紧要,这样就首先排除了选项D。从金属单质与过量酸进行置换反应的化学方程式中可以看出,当金属的物质的量相同时,而金属元素的化合价不同,生成的氢气体积也不同。这种判断是解决本题的重要关键。由上述判断可知,只要知道了V(A)与V(B)之比,就可以知道两种金属元素的化合价。这是因为,若m、n分别是A、B的化合价,下式可以成立:m/n="V(A)/V(B) " 由于A、B两元素的化合价只可能是+1、+2或+3,知道了它们化合价之比,也就可确定出它们的化合价。

练习册系列答案
 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
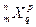 中,m、n、p、q表示某元素的四个角码。若x1与x2的q均为1,m、p对应相等,n不相等,则x1、x2表示的可能是( )
中,m、n、p、q表示某元素的四个角码。若x1与x2的q均为1,m、p对应相等,n不相等,则x1、x2表示的可能是( )