题目内容
醋酸的下列性质中,可以证明它是弱电解质的是( )
| A、醋酸溶液可与纯碱溶液反应产生CO2 |
| B、相同pH的醋酸溶液和盐酸分别跟同样大小颗粒的锌反应时,产生H2的起始速率相等 |
| C、10 mL 1 mol?L-1醋酸溶液恰好与10 mL 1 mol?L-1NaOH溶液完全反应 |
| D、在相同条件下,醋酸溶液的导电性比盐酸溶液的弱 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:证明醋酸是弱电解质的方法有:1.根据醋酸的电离程度,2.根据醋酸的强碱盐溶液的酸碱性判断.
解答:
解:A、强酸和弱酸都可以和纯碱溶液反应产生CO2,不能证明它是弱电解质,故A错误;
B、相同pH的醋酸溶液和盐酸,其氢离子浓度大小一样,所以跟同样大小颗粒的锌反应时,产生H2的起始速率相等,不能证明它是弱电解质,故B错误;
C、10 mL 1 mol?L-1醋酸溶液恰好与10 mL 1 mol?L-1NaOH溶液完全反应,是因为二者的物质的量相等,就是10 mL 1 mol?L-1盐酸溶液也是可以恰好与10 mL 1 mol?L-1NaOH溶液完全反应,不能证明它是弱电解质,故C错误;
D、在相同条件下,醋酸溶液的导电性比盐酸溶液的弱,说明醋酸中离子浓度小于盐酸中的离子浓度,醋酸不完全电离,能证明其是弱电解质,故D正确.
故选D.
B、相同pH的醋酸溶液和盐酸,其氢离子浓度大小一样,所以跟同样大小颗粒的锌反应时,产生H2的起始速率相等,不能证明它是弱电解质,故B错误;
C、10 mL 1 mol?L-1醋酸溶液恰好与10 mL 1 mol?L-1NaOH溶液完全反应,是因为二者的物质的量相等,就是10 mL 1 mol?L-1盐酸溶液也是可以恰好与10 mL 1 mol?L-1NaOH溶液完全反应,不能证明它是弱电解质,故C错误;
D、在相同条件下,醋酸溶液的导电性比盐酸溶液的弱,说明醋酸中离子浓度小于盐酸中的离子浓度,醋酸不完全电离,能证明其是弱电解质,故D正确.
故选D.
点评:本题考查了弱电解质的判断,可以从以下方面判断电解质是否是弱电解质:电离平衡方面、水解方面、离子浓度方面.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
下列实验操作或方法中,不正确的是( )
A、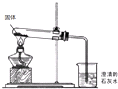 区别碳酸钠和碳酸氢钠 |
B、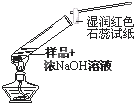 检验试液中NH4+的存在 |
C、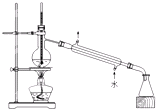 实验室蒸馏石油 |
D、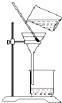 过滤操作 |
现在配制100mL 1mol/L NaOH溶液,下列操作正确的是( )
| A、在托盘天平的两个托盘上各放一张大小一样的纸,然后将氢氧化钠固体放在纸片上进行称量 |
| B、用蒸馏水洗涤烧杯、玻璃棒2-3次,每次洗涤后的溶液都注入容量瓶中 |
| C、把称量的NaOH固体放入盛有适量蒸馏水的烧杯中,溶解后立即把溶液移入100mL容量瓶中 |
| D、沿着玻璃棒往容量瓶中加入蒸馏水,直到溶液凹液面恰好与刻度相切 |
对于反应4A+5B?4C+6D来说,以下化学反应速率的表示中,反应速率最快的是( )
| A、V(A)=0.40mol/(L?s) |
| B、V(B)=0.48mol/(L?s) |
| C、V(C)=0.36mol/(L?s) |
| D、V(D)=0.55mol/(L?s) |
下列实验操作错误的是( )
A、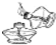 |
B、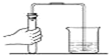 |
C、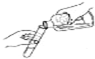 |
D、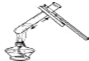 |
下列有关配制一定物质的量浓度溶液的操作,能达到目的是( )
| A、将58.5g NaCl溶于1L水中可得1mol?L-1的NaCl溶液 |
| B、将标准状况下22.4L HCl溶于1L水中可得1mol?L-1盐酸 |
| C、将25.0g胆矾溶于水后配成100mL溶液,所得溶液的物质的量浓度为1mol?L-1 |
| D、将78g Na2O2溶于水得到1L溶液,其物质的量浓度为1mol?L-1 |
下列有关碳酸钠、碳酸氢钠的说法中,正确的是( )
| A、除去碳酸钠固体中混有的少量碳酸氢钠可以采用加热的方法 |
| B、相同条件下,碳酸钠的溶解度小于碳酸氢钠的溶解度 |
| C、碳酸钠与盐酸反应放出二氧化碳的剧烈程度强于碳酸氢钠 |
| D、石灰水能和NaHCO3反应,不与Na2CO3反应 |
下列说法正确的是( )
| A、增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 |
| B、有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C、升高温度能使化学反应速率增大的主要原因是增加了反应物中活化分子的百分数 |
| D、催化剂能增大单位体积内活化分子的百分数,从而增大反应速率 |