题目内容
下列关于强、弱电解质和非电解质的组合完全正确的是( )
| 选项 | 强电解质 | 弱电解质 | 非电解质 |
| A | 纯碱 | 冰醋酸 | 液氯 |
| B | 硫酸 | 重晶石 | 干冰 |
| C | 石灰石 | 蓝矾 | 酒精 |
| D | 硝酸 | 苯甲酸 | 蔗糖 |
| A、A | B、B | C、C | D、D |
考点:强电解质和弱电解质的概念,电解质与非电解质
专题:
分析:强电解质是指在水中完全电离成离子的化合物,主要包括强酸、强碱、大部分盐和活泼金属氧化物;
弱电解质是指在水中不完全电离,只有部分电离的化合物,主要包括弱酸、弱碱、少部分盐和水;
在水溶液里或熔融状态下都不导电的化合物是非电解质,主要包括非金属氧化物、一些氢化物和有机物等,单质和混合物既不是电解质,也不是非电解质.
弱电解质是指在水中不完全电离,只有部分电离的化合物,主要包括弱酸、弱碱、少部分盐和水;
在水溶液里或熔融状态下都不导电的化合物是非电解质,主要包括非金属氧化物、一些氢化物和有机物等,单质和混合物既不是电解质,也不是非电解质.
解答:
解:A、纯碱溶于水能完全电离,所以纯碱是强电解质;冰醋酸在水中只有部分电离,所以属于弱电解质;液氯是氯气单质的液态,氯气是单质,不是化合物,所以氯气不是非电解质,故A错误;
B、H2SO4溶于水能完全电离,所以H2SO4是强电解质;重晶石溶于水能完全电离,所以重晶石是强电解质;CO2自身不能电离出阴阳离子,所以是非电解质,故B错误;
C、溶于水的CaCO3能完全电离,所以CaCO3是强电解质;蓝矾在水中完全电离,所以属于强电解质;乙醇的水溶液不导电,所以是非电解质,故C错误;
D、HNO3溶于水能完全电离,所以HNO3是强电解质;苯甲酸在水中只有部分电离,所以属于弱电解质;蔗糖自身不能电离出阴阳离子,所以是非电解质,故D正确.
故选D.
B、H2SO4溶于水能完全电离,所以H2SO4是强电解质;重晶石溶于水能完全电离,所以重晶石是强电解质;CO2自身不能电离出阴阳离子,所以是非电解质,故B错误;
C、溶于水的CaCO3能完全电离,所以CaCO3是强电解质;蓝矾在水中完全电离,所以属于强电解质;乙醇的水溶液不导电,所以是非电解质,故C错误;
D、HNO3溶于水能完全电离,所以HNO3是强电解质;苯甲酸在水中只有部分电离,所以属于弱电解质;蔗糖自身不能电离出阴阳离子,所以是非电解质,故D正确.
故选D.
点评:本题考查了强电解质、弱电解质和非电解质的判断,明确电解质的强弱与电离程度有关,与溶解能力大小无关.

练习册系列答案
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案
相关题目
下列实验操作中不正确的是( )
| A、用容量瓶配制一定物质的量浓度的NaOH溶液时,溶解后的溶液要马上转移至容量瓶 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、蒸发结晶时当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干 |
| D、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
 的同分异构体中,苯环上的一氯代物只有两种的结构有( )
的同分异构体中,苯环上的一氯代物只有两种的结构有( )| A、1种 | B、2种 | C、3种 | D、4种 |
同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3、②NO2进行喷泉实验,经充分反应后,两瓶内溶液的物质的量浓度大小为( )
| A、①>② | B、①<② |
| C、①=② | D、不能确定 |
如图各装置中,均为电解液,不能构成原电池的是( )
A、 |
B、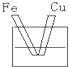 |
C、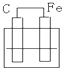 |
D、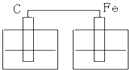 |
下列物质中属于强电解质的是( )
| A、二氧化硅 | B、碳酸钙 |
| C、氢氧化铜 | D、浓硫酸 |
下列描述,其因果关系成立的是( )
| A、因为NH3的水溶液可以导电,所以NH3是电解质 |
| B、因为Cl2可以使湿润的有色布条褪色,所以Cl2具有漂白性 |
| C、因为液态HCl不导电,所以HCl是非电解质 |
| D、因为氢氧化铁胶体具有吸附性,所以常用于净水 |
下列关于晶体与非晶体的说法不正确的是( )
| A、晶体具有固定的熔沸点 |
| B、晶体具有各向异性 |
| C、许多玻璃制品具有规则的几何外形,所以玻璃属于晶体 |
| D、区分晶体和非晶体最可靠的方法是对固体进行X-射线衍射实验 |
下列图式表示正确的是( )
A、二氧化碳 |
| B、次氯酸的结构式 H-Cl-O |
| C、铁离子的价电子排布式 3d34s2 |
D、氯化铯的晶体结构  |