题目内容
同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3、②NO2进行喷泉实验,经充分反应后,两瓶内溶液的物质的量浓度大小为( )
| A、①>② | B、①<② |
| C、①=② | D、不能确定 |
考点:含氮物质的综合应用,物质的量浓度的相关计算,氨的化学性质
专题:氮族元素
分析:设烧瓶体积为VL,①中溶液体积等于氨气的体积等于烧瓶的体积,根据气体的体积求出物质的量,再求出浓度;
②中发生反应:3NO2+2H2O=2HNO3+NO,根据气体的物质的量求出硝酸的物质的量,再根据溶液的体积求出浓度.
②中发生反应:3NO2+2H2O=2HNO3+NO,根据气体的物质的量求出硝酸的物质的量,再根据溶液的体积求出浓度.
解答:
解:同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3、②NO2,进行喷泉实验,经充分反应后,
设烧瓶体积为VL,
①中溶液体积等于氨气的体积,溶液物质的量浓度=
=
mol/L;
②中发生反应:3NO2+2H2O=2HNO3+NO,3体积二氧化氮反应得到1体积NO,硝酸溶液体积为NO2体积的
,NO2的体积为VL,则生成硝酸的物质的量为
×
mol,故硝酸溶液浓度=
=
mol/L,
故溶液的物质的量浓度为①=②,
故选C.
设烧瓶体积为VL,
①中溶液体积等于氨气的体积,溶液物质的量浓度=
| ||
| VL |
| 1 |
| 22.4 |
②中发生反应:3NO2+2H2O=2HNO3+NO,3体积二氧化氮反应得到1体积NO,硝酸溶液体积为NO2体积的
| 2 |
| 3 |
| 2 |
| 3 |
| V |
| 22.4 |
| ||||
|
| 1 |
| 22.4 |
故溶液的物质的量浓度为①=②,
故选C.
点评:本题考查了喷泉实验,侧重于物质的量浓度的计算的考查,题目难度不大,注意把握溶液体积的计算.

练习册系列答案
相关题目
下面关于金属钠的描述正确的是( )
| A、Na2O和Na2O2中阴阳离子个数比都为1:2 |
| B、钠离子和钠原子都具有较强的还原性 |
| C、钠能把钛锆等金属从它们的盐溶液中还原出来 |
| D、钠和钾的合金于室温下呈固态,可做原子反应堆的导热剂 |
用3g铁屑与适量3mol/L稀硫酸反应制取H2气体,若要增大反应速率,可采取的措施是( ):
①再加入适量1mol/L硫酸 ②再加入适量3mol/L硫酸 ③改用3g铁粉 ④适当升高温度 ⑤加几滴CuSO4溶液 ⑥用98%浓硫酸代替1mol/L稀硫酸.
①再加入适量1mol/L硫酸 ②再加入适量3mol/L硫酸 ③改用3g铁粉 ④适当升高温度 ⑤加几滴CuSO4溶液 ⑥用98%浓硫酸代替1mol/L稀硫酸.
| A、①④⑤ | B、②③④ |
| C、③④⑤ | D、③④⑥ |
红热的木炭与浓HNO3反应产生的气体经如下处理:
气体产物
气体Ⅰx mL
气体Ⅱy mL(在无氧环境下操作)假设气体体积均在相同状况下测定,不考虑气体的溶解,则x和y的关系是( )
气体产物
| 浓H2SO4干燥 |
| ①足量饱和NaHCO3溶液 |
| ②浓H2SO4干燥 |
A、x=
| ||
B、y=
| ||
| C、x=y | ||
D、y=
|
下列说法不正确的是( )
| A、放热反应不需加热即可发生 |
| B、化学反应过程中的能量变化除了热能外,也可以是光能、电能等 |
| C、需要加热才能进行的化学反应不一定是吸热反应 |
| D、反应物的总能量大于生成物的总能量为放热反应 |
能说明X的非金属性比Y的强的是( )
| A、X的最高价氧化物的水化物的碱性比Y的最高价氧化物的水化物的碱性强 |
| B、X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强 |
| C、与H2化合时X单质不如Y单质容易 |
| D、Y单质可以X把从其氢化物中置换出来 |
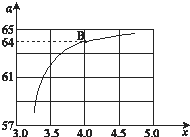 工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+CO2 (g?CO(NH2)2 (l)+H2O (l),该反应的平衡常数和温度关系如下:
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+CO2 (g?CO(NH2)2 (l)+H2O (l),该反应的平衡常数和温度关系如下: