题目内容
.已知A、B、C、D都是短周期元素,它们的原子半径大小为B>C>D>A。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子有2个未成对电子。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体。E的硫酸盐溶液是制备波尔多液的原料之一。回答下列问题(用元素符号或化学式表示)。
(1)M分子中B原子轨道的杂化类型为 ,1mol M中含有σ键的数目为 。
(2)化合物CA3的沸点比化合物BA4的高,其主要原因是 。
(3)写出与BD2互为等电子体的C3-的结构式 。
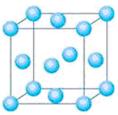
(4)E+的核外电子排布式为 ,下图是E的某种氧化物的晶胞结构示意图,氧的配位数为 。

(5)向E的硫酸盐溶液中通入过量的CA3,写出该反应的离子方程式: 。
(1)M分子中B原子轨道的杂化类型为 ,1mol M中含有σ键的数目为 。
(2)化合物CA3的沸点比化合物BA4的高,其主要原因是 。
(3)写出与BD2互为等电子体的C3-的结构式 。
(4)E+的核外电子排布式为 ,下图是E的某种氧化物的晶胞结构示意图,氧的配位数为 。

(5)向E的硫酸盐溶液中通入过量的CA3,写出该反应的离子方程式: 。
(1)sp2 3NA(或3×6.02×1023) (2分)
(2)NH3分子间能形成氢键 (2分)
(3)[N=N=N]- (2分)
(4)1s22s22p63s23p63d10 4 (每空2分)
(5)Cu2++4NH3=[Cu(NH3) 4]2+ (2分)
(2)NH3分子间能形成氢键 (2分)
(3)[N=N=N]- (2分)
(4)1s22s22p63s23p63d10 4 (每空2分)
(5)Cu2++4NH3=[Cu(NH3) 4]2+ (2分)
略

练习册系列答案
相关题目
 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物,其晶胞结构如右图。
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物,其晶胞结构如右图。