题目内容
【题目】化合物H是重要的有机物,可由E和F在一定条件下合成:(部分反应物或产物省略,另请注意箭头的指向)
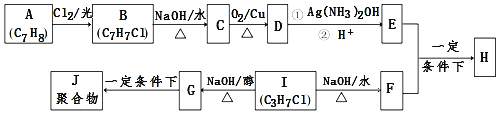
已知以下信息:
i.A属于芳香烃,H属于酯类化合物.
ii.I的核磁共振氢谱为二组峰,且峰的面积比为6:1.
回答下列问题:
(1)B的结构简式_____.
(2)B→C和G→J两步的反应类型_____,_____.
(3)①E+F→H的化学方程式_____.
②D与银氨溶液反应的化学方程式_____.
(4)I的同系物K比I相对分子质量大28,K有多种同分异构体.
①K的同分异构体共_____种.
②若K不能发生消去反应,则K的结构简式为_____.
【答案】 ![]() 取代反应 加聚反应
取代反应 加聚反应 ![]()
![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
![]() +2Ag↓+3NH3+H2O 8 (CH3)3CCH2Cl
+2Ag↓+3NH3+H2O 8 (CH3)3CCH2Cl
【解析】分析:A属于芳香烃,分子式为C7H8,则A为![]() ,A与氯气在光照条件下发生甲基上取代反应生成B,结合B的分子式可知B为
,A与氯气在光照条件下发生甲基上取代反应生成B,结合B的分子式可知B为![]() ,B发生水解反应生成C为
,B发生水解反应生成C为![]() ,C发生催化氧化生成D为
,C发生催化氧化生成D为![]() ,D与银氨溶液反应、酸化得到E为
,D与银氨溶液反应、酸化得到E为![]() 。I的分子式为C3H7Cl,核磁共振氢谱为二组峰,且峰的面积比为6:1,则I为CH3CHClCH3,I发生水解反应得到F为CH3CH(OH)CH3,E与F发生酯化反应生成H为
。I的分子式为C3H7Cl,核磁共振氢谱为二组峰,且峰的面积比为6:1,则I为CH3CHClCH3,I发生水解反应得到F为CH3CH(OH)CH3,E与F发生酯化反应生成H为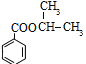 。I发生消去反应生成G为CH2=CHCH3,G发生加聚反应生成J为
。I发生消去反应生成G为CH2=CHCH3,G发生加聚反应生成J为![]() ,据此解答。
,据此解答。
详解:(1)通过以上分析可知B结构简式为![]() 。
。
(2)通过以上分析可知B→C和G→J两步的反应类型分别为取代反应、加聚反应。
(3)①通过以上分析可知E+F→H的化学方程式为:![]() ;
;
②D与银氨溶液反应的化学方程式为![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
![]() +2Ag↓+3NH3+H2O;
+2Ag↓+3NH3+H2O;
(4)I(CH3CHClCH3)的同系物K比I相对分子质量大28,则K的分子式为C5H11Cl。
①K可以看作C5H12被氯原子取代的产物,正戊烷被取代有3种,异戊烷被取代有4种,新戊烷被取代有1种,故K的同分异构体有8种。
②若K不能发生去反应,则K的结构简式为(CH3)3CCH2Cl。

 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案