题目内容
【题目】醋酸亚铬晶体是一种氧气吸收剂,化学式为[Cr(CH3COO)2]22H2O,不溶于冷水,易溶于盐酸.由于Cr2+易被氧气氧化,制备醋酸亚铬时,需在封闭体系中用锌作还原剂,先将Cr3+还原为Cr2+,再与醋酸钠溶液作用制得,其总反应为:2Cr3++Zn+4CH3COO﹣+2H2O═[Cr(CH3COO)2]22H2O+Zn2+。请回答下列问题:

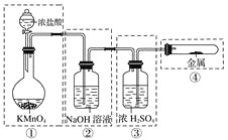
(1)实验中用恒压滴液漏斗,相比普通分液漏斗,显著的优点是_______________________.
(2)实验开始前,必需进行的实验操作是________;实验开始时,打开恒压滴液漏斗的旋塞,让盐酸滴入装置2中,打开A,关闭B,目的是___________________________,反应一段时间后,保持盐酸持续滴下,关闭A,打开B,目的是__________________________________.
(3)已知其它反应物足量,实验时取用的是含溶质3.17g CrCl3溶液和1L 0.1molL﹣1的醋酸钠溶液;实验后得干燥纯净的醋酸亚铬晶体2.82g,则该实验所得产品的产率为_____%(不考虑醋酸亚铬晶体的溶解损失).
(4)为标定实验所用的CrCl3溶液,进行了如下操作:
取25.00mLCrCl3溶液于碘量瓶(一种带塞的锥形瓶)中,加热至沸后加入适量Na2O2,充分加热煮沸,稀释,加入过量的稀H2SO4至溶液呈强酸性,此时铬以Cr2O72﹣存在;再加入足量KI,密塞,摇匀,于暗处静置5分钟后,用0.25molL﹣1硫代硫酸钠溶液滴定至溶液呈淡黄色,加入l mL指示剂,滴定至终点.平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL.
已知:Cr2O72﹣+6I﹣+14H+═2Cr3++3I2+7H2O,2S2O32﹣+I2═S4O62﹣十2I﹣.
①实验所用的CrCl3溶液的物质的量浓度为_______.
②滴定过程中所用的指示剂是________.
③下列操作导致实验结果偏低的是___________.
a.移取CrCl3溶液的滴定管,水洗后未用CrCl3溶液润洗
b.盛硫代硫酸钠溶液的滴定管滴定前有气泡,滴定后无气泡
c.量取CrCl3溶液时先俯视后仰视
d.滴定终点时,盛硫代硫酸钠溶液的滴定管尖嘴外挂有一滴液珠未滴落.
【答案】平衡压强,使液体顺利滴下,可以防止液体挥发检验装置的气密性盐酸与锌反应产生的氢气将装置中的空气排出形成还原性氛围,防止Cr2+被氧化让产生的H2将CrCl2溶液压入装置3与CH3COONa溶液反应75%0.08mol/L淀粉溶液ac
【解析】
(1)恒压滴液漏斗优点是平衡压强,使液体顺利滴下,可以防止液体挥发;(2)Cr2+易被氧气氧化,因此制备醋酸亚铬时,首先排除装置的氧气,防止把Cr2+氧化,因此实验前应检验装置的气密性,打开A关闭B其目的是盐酸能与锌反应产生氢气将装置中的空气排出,形成还原性氛围,防止Cr2+被氧化;(3)CrCl3的物质的量为![]() mol=0.02mol,得到CrCl2的物质的量为0.02mol,醋酸钠的物质的量为0.1mol,根据醋酸亚铬晶体的分子式,推出醋酸钠过量,根据元素守恒,[Cr(CH3COO)2]2·2H2O的物质的量为0.01mol,质量为0.01×376g=3.76g,所得产品的产率为
mol=0.02mol,得到CrCl2的物质的量为0.02mol,醋酸钠的物质的量为0.1mol,根据醋酸亚铬晶体的分子式,推出醋酸钠过量,根据元素守恒,[Cr(CH3COO)2]2·2H2O的物质的量为0.01mol,质量为0.01×376g=3.76g,所得产品的产率为![]() 75%;(4)①根据操作建立的关系式为
75%;(4)①根据操作建立的关系式为
2Cr3+~Cr2O72-~3I2~6S2O32-
2 6
25×10-3×c(CrCl3) 24×10-3×0.25,解得c(CrCl3)=0.08mol·L-1;②淀粉遇碘单质变蓝,反应完毕后蓝色褪去,可以用淀粉作指示剂,因此滴定过程中所用的指示剂是淀粉;③a、未用CrCl3润洗,CrCl3溶液被稀释,消耗硫代硫酸钠溶液的体积偏小,故a正确;b、气泡体积计算在消耗硫代硫酸钠溶液体积内,测定浓度偏大,故b错误;c、量取CrCl3溶液时先俯视,液面在读数下方,读数偏小,后仰视,液面在读数上方,读数偏大,则CrCl3溶液的体积偏大,测定其浓度偏小,故c正确;d、外挂有一滴液珠未滴落,以计算在消耗硫代硫酸钠溶液体积内,测定浓度偏大,故d错误。

 名校课堂系列答案
名校课堂系列答案