题目内容
粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥沙等不溶性杂质.我们食用的精盐是用粗食盐提纯而得到的.通常经过以下步骤:
①加入稍过量的BaCl2溶液;②加入稍过量的NaOH溶液;③加入稍过量的Na2CO3溶液;④过滤;⑤滴入稀盐酸至无气泡产生;回答下列问题.
(1)实验室进行NaCl溶液蒸发时,包含以下操作步骤:①固定铁圈位置;②放上蒸发皿(蒸发皿中盛有NaCl溶液);③放置酒精灯;④加热搅拌;⑤停止加热.其正确的操作顺序为 .
(2)如何检验粗盐的提纯步骤①中所加BaCl2溶液是否过量? .
(3)步骤③加入稍过量的Na2CO3溶液,直至不再产生沉淀为止.请问这步操作的目的是 .
(4)步骤④为过滤操作.请问这一操作能除掉哪些杂质? .
(5)步骤⑤滴入稀盐酸至无气泡产生,写出这一步发生的所有化学方程式: .
①加入稍过量的BaCl2溶液;②加入稍过量的NaOH溶液;③加入稍过量的Na2CO3溶液;④过滤;⑤滴入稀盐酸至无气泡产生;回答下列问题.
(1)实验室进行NaCl溶液蒸发时,包含以下操作步骤:①固定铁圈位置;②放上蒸发皿(蒸发皿中盛有NaCl溶液);③放置酒精灯;④加热搅拌;⑤停止加热.其正确的操作顺序为
(2)如何检验粗盐的提纯步骤①中所加BaCl2溶液是否过量?
(3)步骤③加入稍过量的Na2CO3溶液,直至不再产生沉淀为止.请问这步操作的目的是
(4)步骤④为过滤操作.请问这一操作能除掉哪些杂质?
(5)步骤⑤滴入稀盐酸至无气泡产生,写出这一步发生的所有化学方程式:
考点:粗盐提纯
专题:实验题
分析:(1)组装仪器的一般顺序是采用先左后右,先下后上的原则,利用本规则即可解答.
(2)要除去杂质,需加入过量的除杂物质,要判断BaCl2是否过量,可取少量上层清液,继续滴加BaCl2溶液,观察现象;
(3)加入稍过量的Na2CO3溶液的目的是除去Ca2+和过量的Ba2+;
(4)过滤能实现固液分离;
(5)滴入盐酸的目的是除去过量的OH-和CO32-.
(2)要除去杂质,需加入过量的除杂物质,要判断BaCl2是否过量,可取少量上层清液,继续滴加BaCl2溶液,观察现象;
(3)加入稍过量的Na2CO3溶液的目的是除去Ca2+和过量的Ba2+;
(4)过滤能实现固液分离;
(5)滴入盐酸的目的是除去过量的OH-和CO32-.
解答:
解:(1)组装仪器时要从下向上组装,酒精灯在铁圈和蒸发皿的下方,所以要先放酒精灯;然后再固定铁圈,放置蒸发皿;然后再点燃酒精灯加热,并搅拌,当有较多晶体析出时,停止加热,借余热蒸干.故正确的操作顺序是:③①②④⑤;故答案为:③①②④⑤;
(2)要判断BaCl2是否过量,可取少量上层清液,继续滴加BaCl2溶液,如没有白色沉淀出现,则说明BaCl2过量,
故答案为:取少量上层清液于试管中,继续滴加BaCl2溶液,如没有白色沉淀出现,则说明BaCl2过量;
(3)粗盐中本来就有Ca2+,在除硫酸根时加入过量的氯化钡会引入过量的Ba2+,故加入稍过量的Na2CO3溶液的目的是除去Ca2+和过量的Ba2+,
故答案为:除去Ca2+和过量的Ba2+;
(4)过滤能将产生的BaSO4、CaCO3、Mg(OH)2、BaCO3沉淀和粗盐中本身就有的泥沙除去,故答案为:BaSO4、CaCO3、Mg(OH)2、BaCO3、泥沙;
(5)滴入盐酸的目的是除去过量的NaOH和Na2CO3,化学方程式为:NaOH+HCl═NaCl+H2O Na2CO3+2HCl═2NaCl+H2O+CO2,
故答案为:NaOH+HCl═NaCl+H2O; Na2CO3+2HCl═2NaCl+H2O+CO2.
(2)要判断BaCl2是否过量,可取少量上层清液,继续滴加BaCl2溶液,如没有白色沉淀出现,则说明BaCl2过量,
故答案为:取少量上层清液于试管中,继续滴加BaCl2溶液,如没有白色沉淀出现,则说明BaCl2过量;
(3)粗盐中本来就有Ca2+,在除硫酸根时加入过量的氯化钡会引入过量的Ba2+,故加入稍过量的Na2CO3溶液的目的是除去Ca2+和过量的Ba2+,
故答案为:除去Ca2+和过量的Ba2+;
(4)过滤能将产生的BaSO4、CaCO3、Mg(OH)2、BaCO3沉淀和粗盐中本身就有的泥沙除去,故答案为:BaSO4、CaCO3、Mg(OH)2、BaCO3、泥沙;
(5)滴入盐酸的目的是除去过量的NaOH和Na2CO3,化学方程式为:NaOH+HCl═NaCl+H2O Na2CO3+2HCl═2NaCl+H2O+CO2,
故答案为:NaOH+HCl═NaCl+H2O; Na2CO3+2HCl═2NaCl+H2O+CO2.
点评:本题考查了粗盐提纯过程中的仪器的组装、试剂过量的判断和发生的反应,难度不大,熟悉提纯流程是关键.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
在蒸馏实验中,下列叙述不正确的是( )
| A、在蒸馏烧瓶中加入碎瓷片防止暴沸 |
| B、将温度计水银球插入自来水中 |
| C、冷水从冷凝管下口入,上口出 |
| D、收集蒸馏水时,应弃去开始馏出的部分 |
实验室用固态不纯氯化钠(含少量Na2SO4杂质)制取纯净氯化钠固体.下列操作可供选用:
①逐滴加入稀盐酸,调节pH值为5;
②加热溶液蒸干;
③加蒸馏水溶解;
④加入稍过量的Na2CO3溶液;
⑤加入稍过量的BaCl2溶液;
⑥过滤.
上述实验操作的正确顺序应是( )
①逐滴加入稀盐酸,调节pH值为5;
②加热溶液蒸干;
③加蒸馏水溶解;
④加入稍过量的Na2CO3溶液;
⑤加入稍过量的BaCl2溶液;
⑥过滤.
上述实验操作的正确顺序应是( )
| A、①②⑤⑥③④ |
| B、③⑤④⑥①② |
| C、④③⑥⑤①② |
| D、④③⑤⑥②① |
完成如表实验所选择的装置或仪器(夹持装置已略去)正确的是( )
| A | B | C | D | |
| 实验 | 用CCl4提取溴水中的Br2 | 除去乙醇中的苯酚 | 从KI和I2的固体混合物中回收I2 | 配制1000mL0.1000mol?L-1K2Cr2O2溶液 |
| 装置或仪器 |  | 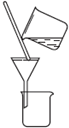 | 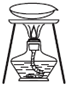 | 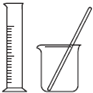 |
| A、A | B、B | C、C | D、D |
取a g某物质在O2中完全燃烧,将生成物与足量Na2O2固体完全反应,反应后,固体质量恰好也增加了a g,下列物质不能满足上述结果的是( )
| A、H2 |
| B、CO |
| C、C6H12O6 |
| D、C12H22O11 |
T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示.则下列结论不正确的是( )


| A、容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g) |
| B、保持其他条件不变,升高温度,反应的化学平衡常数K增大 |
| C、反应进行的前3min内,用X表示的反应速率v(X)=0.1mol/(L?min) |
| D、若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
下列有关化学实验的叙述中,不正确的是( )
| A、重结晶法提纯苯甲酸时,为除去杂质和防止苯甲酸析出,应该趁热过滤 |
| B、除去溴乙烷中溶解的溴,先用足量NaHSO3溶液洗涤分液,再用蒸馏水洗涤分液 |
| C、油脂皂化后可用渗析的方法使高级脂肪酸钠和甘油充分分离 |
| D、盐析可提纯蛋白质并能保持蛋白质的生理活性 |
