题目内容
下表是元素周期表的一部分,表中所列字母分别代表一种元素.

(1)表中的实线表示系周期表的部分边界,请用实线补全元素周期表的上边界
(2)常温下,其单质呈液态的元素是 (填字母代号),它与e形成的化俣物电子式为: (用元素符号表示)
(3)b元素形成的单质所属品体类型可能是 (填序号)
①分子晶体 ②原子晶体 ③金属晶体 ④离子晶体 ⑤过渡型晶体
(4)元素c、d、g的氢化物的沸点由高到低的顺序为 (用化学式表示)
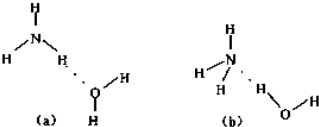
(5)NH3?H2O的电离方程NH3?H2O═NH+4+OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构 (填字母代号)

(1)表中的实线表示系周期表的部分边界,请用实线补全元素周期表的上边界
(2)常温下,其单质呈液态的元素是
(3)b元素形成的单质所属品体类型可能是
①分子晶体 ②原子晶体 ③金属晶体 ④离子晶体 ⑤过渡型晶体
(4)元素c、d、g的氢化物的沸点由高到低的顺序为
(5)NH3?H2O的电离方程NH3?H2O═NH+4+OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构

分析:(1)第一周期中含有2种元素,处于第1列、18列;第2、3周期中元素处于1,2列,13~18列,据此画出元素周期表的上边界;
(2)常温下,呈液态的单质为溴与金属汞,由图可知位置可知,为溴单质,处于第四周期17列;
e为Na元素,溴与钠形成的化合物为NaBr,由钠离子与氯离子构成;
(3)b为碳元素,形成的单质可能为原子晶体,如金刚石,可能为分子晶体,若富勒烯,可能为过渡型晶体,如石墨;
(4)c为氧元素、d为氟元素、g为氯元素,结合常温下氢化物状态与氢键判断氢化物的沸点;
(5)氨水的电离生成NH4+、OH-,说明NH3?H2O 中O-H键发生断裂,来确定氨水的结构和成键情况;
(2)常温下,呈液态的单质为溴与金属汞,由图可知位置可知,为溴单质,处于第四周期17列;
e为Na元素,溴与钠形成的化合物为NaBr,由钠离子与氯离子构成;
(3)b为碳元素,形成的单质可能为原子晶体,如金刚石,可能为分子晶体,若富勒烯,可能为过渡型晶体,如石墨;
(4)c为氧元素、d为氟元素、g为氯元素,结合常温下氢化物状态与氢键判断氢化物的沸点;
(5)氨水的电离生成NH4+、OH-,说明NH3?H2O 中O-H键发生断裂,来确定氨水的结构和成键情况;
解答:解:(1)第一周期中含有2种元素,处于第1列、18列;第2、3周期中元素处于1,2列,13~18列,故元素周期表的上边界为: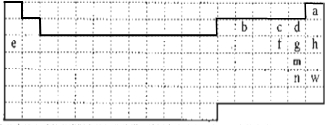 ,
,
故答案为: ;
;
(2)常温下,呈液态的单质为溴与金属汞,由图可知位置可知,为溴单质,处于第四周期17列,为表中m元素;
e为Na元素,溴与钠形成的化合物为NaBr,由钠离子与氯离子构成,溴化钠电子式为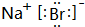 ,
,
故答案为:m;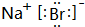 ;
;
(3)b为碳元素,形成的单质可能为原子晶体,如金刚石,可能为分子晶体,若富勒烯,可能为过渡型晶体,如石墨,
故答案为:①②⑤;
(4)c为氧元素、d为氟元素、g为氯元素,常温下水为液体,HF、HCl为气体,故水的沸点较高,HF中分子之间存在氢键,沸点比HCl高,故沸点H2O>HF>HCl,
故答案为:H2O>HF>HCl;
(5)NH3溶于水后,形成的NH3?H2O中,根据NH3?H2O的电离方程式为NH3?H2O?NH4++OH-,可知结构中含有铵根和氢氧根的基本结构,故NH3?H2O结构为b
故答案为:b.
 ,
,故答案为:
 ;
;(2)常温下,呈液态的单质为溴与金属汞,由图可知位置可知,为溴单质,处于第四周期17列,为表中m元素;
e为Na元素,溴与钠形成的化合物为NaBr,由钠离子与氯离子构成,溴化钠电子式为
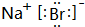 ,
,故答案为:m;
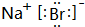 ;
;(3)b为碳元素,形成的单质可能为原子晶体,如金刚石,可能为分子晶体,若富勒烯,可能为过渡型晶体,如石墨,
故答案为:①②⑤;
(4)c为氧元素、d为氟元素、g为氯元素,常温下水为液体,HF、HCl为气体,故水的沸点较高,HF中分子之间存在氢键,沸点比HCl高,故沸点H2O>HF>HCl,
故答案为:H2O>HF>HCl;
(5)NH3溶于水后,形成的NH3?H2O中,根据NH3?H2O的电离方程式为NH3?H2O?NH4++OH-,可知结构中含有铵根和氢氧根的基本结构,故NH3?H2O结构为b
故答案为:b.
点评:本题考查元素周期表与周期律的综合应用,内容涉及电子式、晶体类型、氢键等,注重常考考点的考查,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目



 NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是 (4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是
(4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是