题目内容
(2010?诸城市模拟)化学与生产生活密切相关,下列说法不正确的是( )
分析:A、从胶体性质考虑,血液属于胶体,可利用渗析的方法分离胶体和溶液;
B、根据明矾净水的原理和漂白粉的净水原理来回答;
C、根据原电池的构成条件来回答;
D、根据玻璃、陶瓷、水泥的生成原料知识来分析.
B、根据明矾净水的原理和漂白粉的净水原理来回答;
C、根据原电池的构成条件来回答;
D、根据玻璃、陶瓷、水泥的生成原料知识来分析.
解答:解:A、血液属于胶体,不能透过半透膜,可利用渗析的方法分离胶体和溶液,血透的原理是利用渗析的方法净化血液,故A正确;
B、明矾净水的原理是铝离子水解生成的氢氧化铝具有净水作用,漂白粉的漂白原理是次氯酸的漂白性导致,二者常用于自来水的净化和杀菌消毒,其作用原理不相同,故B错误;
C、钢铁中的铁、碳和潮湿的空气构成原电池,铁为负极,易发生电化学腐蚀中的吸氧腐蚀,故C正确;
D、玻璃、陶瓷、水泥中主要成分是硅酸盐,均属于无机硅酸盐材料,其生产原料都需要石灰石,故D正确.
故选B.
B、明矾净水的原理是铝离子水解生成的氢氧化铝具有净水作用,漂白粉的漂白原理是次氯酸的漂白性导致,二者常用于自来水的净化和杀菌消毒,其作用原理不相同,故B错误;
C、钢铁中的铁、碳和潮湿的空气构成原电池,铁为负极,易发生电化学腐蚀中的吸氧腐蚀,故C正确;
D、玻璃、陶瓷、水泥中主要成分是硅酸盐,均属于无机硅酸盐材料,其生产原料都需要石灰石,故D正确.
故选B.
点评:本题考查较为综合,涉及物质的漂白性、工业生产、电化学腐蚀等知识,题目难度不大,注意胶体的性质、水的净化和消毒等问题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
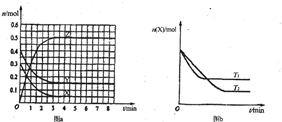 (2010?诸城市模拟)T0℃时,在2L的密闭容器中发生反应:aX(g)+bY(g)?cZ(g),各物质的物质的量随时间变化的关系如图a所示.其他条件相同,温度分别为T1℃、T2℃时发生反应,X的物质的量随时间变化的关系如图b所示.下列叙述不正确的是( )
(2010?诸城市模拟)T0℃时,在2L的密闭容器中发生反应:aX(g)+bY(g)?cZ(g),各物质的物质的量随时间变化的关系如图a所示.其他条件相同,温度分别为T1℃、T2℃时发生反应,X的物质的量随时间变化的关系如图b所示.下列叙述不正确的是( )


