题目内容
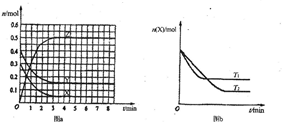 (2010?诸城市模拟)T0℃时,在2L的密闭容器中发生反应:aX(g)+bY(g)?cZ(g),各物质的物质的量随时间变化的关系如图a所示.其他条件相同,温度分别为T1℃、T2℃时发生反应,X的物质的量随时间变化的关系如图b所示.下列叙述不正确的是( )
(2010?诸城市模拟)T0℃时,在2L的密闭容器中发生反应:aX(g)+bY(g)?cZ(g),各物质的物质的量随时间变化的关系如图a所示.其他条件相同,温度分别为T1℃、T2℃时发生反应,X的物质的量随时间变化的关系如图b所示.下列叙述不正确的是( )分析:A、结合图b根据先拐先平数值大原则,判断温度高低,再根据平衡时X的物质的量判断反应热效应.
B、结合图a判断X、Y、Z的物质的量变化,根据速率之比等于物质的量变化量之比判断.
C、由图a可知Y的物质的量变化量为0.25mol,开始时Y的物质的量为0.4mol,再利用转化率的定义计算.
D、升高温度平衡向吸热反应移动,据此判断.
B、结合图a判断X、Y、Z的物质的量变化,根据速率之比等于物质的量变化量之比判断.
C、由图a可知Y的物质的量变化量为0.25mol,开始时Y的物质的量为0.4mol,再利用转化率的定义计算.
D、升高温度平衡向吸热反应移动,据此判断.
解答:解:A、由图b可知,温度为T1先到达平衡,所以T1>T2,温度越高,平衡时X的物质的量越大,说明升高温度平衡向逆反应移动,升高温度平衡向吸热反应移动,故正反应为放热反应,故A正确;
B、由图a可知到达平衡时,X、Y、Z的物质的量变化量分别为0.25mol、0.25mol、0.5mol,速率之比等于物质的量变化量之比,所以X、Y、Z的化学反应速率之比为1:1:2,故B正确;
C、图a中反应达到平衡时,参加反应的Y的物质的量为0.25mol,开始时Y的物质的量为0.4mol,所以平衡时Y的转化率为
×100%=62.5%,故C错误;
D、由A分析可知,该正反应为放热反应,若T1>T0,升高温度平衡向吸热反应移动,即向逆反应移动,平衡常数减小,即
化学平衡常数K(T1)<K(T0),故D正确.
故选:D.
B、由图a可知到达平衡时,X、Y、Z的物质的量变化量分别为0.25mol、0.25mol、0.5mol,速率之比等于物质的量变化量之比,所以X、Y、Z的化学反应速率之比为1:1:2,故B正确;
C、图a中反应达到平衡时,参加反应的Y的物质的量为0.25mol,开始时Y的物质的量为0.4mol,所以平衡时Y的转化率为
| 0.25mol |
| 0.4mol |
D、由A分析可知,该正反应为放热反应,若T1>T0,升高温度平衡向吸热反应移动,即向逆反应移动,平衡常数减小,即
化学平衡常数K(T1)<K(T0),故D正确.
故选:D.
点评:以图象为载体考查反应速率、外界条件对反应速率的影响、平衡常数等,难度不大,注意平衡图象先拐先平数值大原则与定一议二原则.

练习册系列答案
相关题目