题目内容
下列物质:(1)Na (2)液溴 (3)Na2O (4)NO2 (5)干冰 (6)甲烷 (7)氨水(8)氢硫酸 (9)HCl气体 (10)硫酸 (11)熔融NaOH (12)蔗糖 (13)NaCl溶液 (14)AgCl (15)胆矾
属于电解质的是 ,属于非电解质的是 ,能导电的是 .
属于电解质的是
考点:电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:①根据电解质在熔融状态或水溶液中能导电的化合物,包括酸、碱、盐、氧化物等化合物;
②非电解质在熔融状态和水溶液中都不能导电的化合物,包括非金属氧化物、氨气、少数有机物如蔗糖、乙醇等;
单质,混合物不管在水溶液中或熔融状态下能够导电与否,都不是电解质或非电解质;
③能导电的物质--必须具有能自由移动的带电的微粒,金属能导电--是由于金属中存在能自由移动的带负电的电子.
②非电解质在熔融状态和水溶液中都不能导电的化合物,包括非金属氧化物、氨气、少数有机物如蔗糖、乙醇等;
单质,混合物不管在水溶液中或熔融状态下能够导电与否,都不是电解质或非电解质;
③能导电的物质--必须具有能自由移动的带电的微粒,金属能导电--是由于金属中存在能自由移动的带负电的电子.
解答:
解::(1)Na是单质,既不是电解质,也不是非电解质,能导电;
(2)液溴是单质,既不是电解质,也不是非电解质,由原子构成,不能导电;
(3)Na2O熔融时电离生成钠离子和氧离子,是电解质,不导电;
(4)NO2是非金属氧化物,属于非电解质,没有离子,不导电;
(5)干冰是非金属氧化物,属于非电解质,没有离子,不导电;
(6)甲烷不能发生电离,属于非电解质,没有离子,不导电;
(7)氨水属于混合物,既不是电解质,也不是非电解质,溶液中含有阴阳离子,能导电;
(8)氢硫酸属于混合物,既不是电解质,也不是非电解质,溶液中含有阴阳离子,能导电;
(9)HCl气体溶于水能自身电离出自由移动的离子而导电,是电解质,但气体本身不能够导电;
(10)硫酸溶于水能自身电离出自由移动的离子而导电,是电解质,由原子构成,不能导电;
(11)熔融NaOH是强碱,是电解质,其中含有自由移动的阴阳离子,可以导电;
(12)蔗糖自身不能发生电离,是非电解质,由原子构成,不能导电;
(13)NaCl溶液是混合物,既不是电解质,也不是非电解质,有自由移动的离子,能导电;
(14)AgCl熔融态能发生电离,是电解质,AgCl固体中离子不能自由移动,不导电;
(15)胆矾是盐,溶于水能发生电离,是电解质,胆矾中离子不能自由移动,不导电;
因此属于电解质的是(3)(9)(10)(11)(14)(15),属于非电解质的是(4)(5)(6)(12),能导电的是(1)(7)(8)(11)(13).
故答案为:(3)(9)(10)(11)(14)(15);(4)(5)(6)(12);(1)(7)(8)(11)(13).
(2)液溴是单质,既不是电解质,也不是非电解质,由原子构成,不能导电;
(3)Na2O熔融时电离生成钠离子和氧离子,是电解质,不导电;
(4)NO2是非金属氧化物,属于非电解质,没有离子,不导电;
(5)干冰是非金属氧化物,属于非电解质,没有离子,不导电;
(6)甲烷不能发生电离,属于非电解质,没有离子,不导电;
(7)氨水属于混合物,既不是电解质,也不是非电解质,溶液中含有阴阳离子,能导电;
(8)氢硫酸属于混合物,既不是电解质,也不是非电解质,溶液中含有阴阳离子,能导电;
(9)HCl气体溶于水能自身电离出自由移动的离子而导电,是电解质,但气体本身不能够导电;
(10)硫酸溶于水能自身电离出自由移动的离子而导电,是电解质,由原子构成,不能导电;
(11)熔融NaOH是强碱,是电解质,其中含有自由移动的阴阳离子,可以导电;
(12)蔗糖自身不能发生电离,是非电解质,由原子构成,不能导电;
(13)NaCl溶液是混合物,既不是电解质,也不是非电解质,有自由移动的离子,能导电;
(14)AgCl熔融态能发生电离,是电解质,AgCl固体中离子不能自由移动,不导电;
(15)胆矾是盐,溶于水能发生电离,是电解质,胆矾中离子不能自由移动,不导电;
因此属于电解质的是(3)(9)(10)(11)(14)(15),属于非电解质的是(4)(5)(6)(12),能导电的是(1)(7)(8)(11)(13).
故答案为:(3)(9)(10)(11)(14)(15);(4)(5)(6)(12);(1)(7)(8)(11)(13).
点评:本题考查电解质和非电解质的概念,电解质导电的原因,难度中等,解题的关键是明确电解质和非电解质的本质区别.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
以下有关元素性质的说法不正确的是( )
| A、具有下列电子排布式的原子中,①1s22s22p63s23p2②1s22s22p3③1s22s22p2④1s222s2p63s23p4原子半径最大的是① |
| B、具有下列价电子排布式的原子中,①3s23p1②3s23p2③3s23p3④3s23p4 第一电离能最大是③ |
| C、①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的电负性随原子序数增大而递增的是④ |
| D、某元素气态基态原子的逐级电离能分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X3+ |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、25°C时,1L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA |
| B、标准状况下,1molCF4中含有的电子对数目为4.0NA |
| C、1L 0.5mol?L-1 的H2SO3溶液中含有的H+数目为NA |
| D、一定条件下1molN2与3molH2混合充分反应后生成NH3分子数小于2.0NA |
在密闭容器中进行如下反应:X2(气)+Y2(气)?2Z(气),已知 X2、Y2、Z的起始浓度分别为 0.1mol/L,0.3mol/L,0.2mol/L,在一定的条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A、Y2为0.2 mol/L |
| B、Y2 为0.35 mol/L |
| C、X2 为0.2 mol/L |
| D、Z为 0.4 mol/L |
关于氢键,下列说法正确的是( )
| A、含氢元素的化合物中一定有氢键 |
B、因为分子间存在氢键的缘故,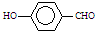 比 比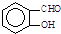 熔沸点高 熔沸点高 |
| C、由于氢键比范德华力强,所以H2O分子比H2S分子稳定 |
| D、“可燃冰”--甲烷水合物(例如:8CH4?46H2O)中CH4与H2O之间存在氢键 |
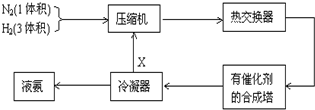 如图是合成氨的简要流程示意图,沿X路线回去的物质是( )
如图是合成氨的简要流程示意图,沿X路线回去的物质是( )| A、N2和H2 |
| B、催化剂 |
| C、NH3 |
| D、H2 |