题目内容
下列物质或离子组能大量共存,且满足相应条件的是( )
| 离子或物质 | 条件 | |
| A | SO2、O2、NO2 | 通入足量NaOH溶液后,可能没有任何气体剩余 |
| B | Fe3+、SO32-、Cl- | 加入NaOH溶液,产生红褐色沉淀 |
| C | Ba2+、HCO3-、Cl-、H+ | 加入氨水立即产生沉淀 |
| D | Na+、K+、Cl-、SO42- | c(Na+)+c(K+)=c(SO42-)+c(Cl-) |
| A、A | B、B | C、C | D、D |
考点:离子共存问题
专题:
分析:A.O2、NO2以1:4在水中反应恰好转化为硝酸,二氧化硫与NaOH反应生成盐和水;
B.Fe3+、SO32-发生氧化还原反应生成硫酸亚铁;
C.加入氨水先与H+反应;
D.不遵循电荷守恒.
B.Fe3+、SO32-发生氧化还原反应生成硫酸亚铁;
C.加入氨水先与H+反应;
D.不遵循电荷守恒.
解答:
解:A.O2、NO2以1:4在水中反应恰好转化为硝酸,二氧化硫与NaOH反应生成盐和水,则混合气体通入足量NaOH溶液后,可能没有任何气体剩余,故A正确;
B.Fe3+、SO32-发生氧化还原反应生成硫酸亚铁,铁离子少量时,加NaOH不能立即生成红褐色沉淀,故B错误;
C.加入氨水先与H+反应,再与Ba2+、HCO3-反应,不能立即生成沉淀,故C错误;
D.不遵循电荷守恒,电荷守恒式为c(Na+)+c(K+)=2c(SO42-)+c(Cl-),故D错误;
故选A.
B.Fe3+、SO32-发生氧化还原反应生成硫酸亚铁,铁离子少量时,加NaOH不能立即生成红褐色沉淀,故B错误;
C.加入氨水先与H+反应,再与Ba2+、HCO3-反应,不能立即生成沉淀,故C错误;
D.不遵循电荷守恒,电荷守恒式为c(Na+)+c(K+)=2c(SO42-)+c(Cl-),故D错误;
故选A.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应及氧化还原反应的离子共存考查,注意电荷守恒及反应的先后顺序,题目难度不大.

练习册系列答案
相关题目
某同学按如图所示的装置进行实验,A、B为常见金属,它们的硫酸盐可溶于水.当K闭合时,阴离子交换膜处的SO42-从右向左移动.下列分析正确的是( )
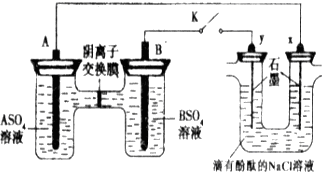

| A、A的金属活动性弱于B |
| B、Na+从y电极趋向x电极 |
| C、Y电极附近溶液先变红 |
| D、B的电极反应:B-2e-=B2+ |
下列说法正确的是( )
| A、液态HCl不导电,所以HCl是非电解质 |
| B、NH3、CO2的水溶液均导电,所以NH3、CO2均是电解质 |
| C、铜、石墨均导电,所以它们都是电解质 |
| D、蔗糖在水溶液中或熔融时均不导电,所以是非电解质 |
与100mL 0.1mol/L的NaCl溶液中Cl-离子浓度相同的是( )
| A、50 mL 0.2 mol/L的NaCl溶液 |
| B、50 mL 0.05 mol/L的MgCl2溶液 |
| C、50 mL 0.2 mol/L的HCl溶液 |
| D、100 mL 0.2 mol/L的KCl溶液 |
下列反应的离子方程式中正确的是( )
| A、铁与盐酸的反应:2Fe+6H+=2Fe3++3H2↑ |
| B、石灰石与稀盐酸反应制备二氧化碳:CO32-+2H+=H2O+CO2↑ |
| C、向氢氧化铜中滴加硫酸溶液:H++OH-=H2O |
| D、硫酸铜溶液和氢氧化钡溶液混合:Cu2++SO42-+Ba2++2OH-=Cu(OH)2↓+BaSO4↓ |
在相同温度下,在体积相同的两个密闭容器内充入等质量的CO2和SO2气体,则下列说法正确的是( )
| A、CO2和SO2中物质的量比为 1:1 |
| B、CO2和SO2的密度比为1:1 |
| C、CO2和SO2的物质的量浓度比为11:16 |
| D、CO2和SO2中所含氧原子个数比为1:1 |