题目内容
A、B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,C为气体,D为固体且C、D含有相同的元素.反应②是炼铁工业中的主要反应,如图是它们之间的相互转化关系.请回答:
(1)填写化学式:A、 B、 C、 D、 E、 F、
(2)写出反应①的离子反应方程式 .

(1)填写化学式:A、
(2)写出反应①的离子反应方程式
考点:无机物的推断,常见金属元素的单质及其化合物的综合应用
专题:推断题,几种重要的金属及其化合物
分析:A、B、C、D、E、F、G为常见的物质,B、E、G属于单质,且E为红色,可推知E为Cu,与氧气反应得到A为CuO,A与过量的稀盐酸反应得到X为CuCl2.C为气体,D为固体且C、D含有相同的元素,反应②是炼铁工业中的主要反应,应是Fe2O3+3CO
2Fe+3CO2,可推知B为Fe、C为CO2、D为Fe2O3 Y为CO,反应①中,铁与过量盐酸反应产生G为氢气,Fe与氯化铜反应得到Cu与F,F为FeCl2,据此解答.
| ||
解答:
解:A、B、C、D、E、F、G为常见的物质,B、E、G属于单质,且E为红色,可推知E为Cu,与氧气反应得到A为CuO,A与过量的稀盐酸反应得到X为CuCl2.C为气体,D为固体且C、D含有相同的元素,反应②是炼铁工业中的主要反应,应是Fe2O3+3CO
2Fe+3CO2,可推知B为Fe、C为CO2、D为Fe2O3 Y为CO,反应①中,铁与过量盐酸反应后溶液中还有FeCl2溶液和过量的盐酸,Fe与氯化铜反应得到Cu与FeCl2,Fe与盐酸反应得到FeCl2与H2,F为FeCl2,G为
H2,
(1)由上述分析可知,A为CuO,B为Fe,C为CO2,D为Fe2O3,E为Cu,F为FeCl2,
故答案为:CuO;Fe;CO2;Fe2O3;Cu;FeCl2;
(2)反应①的离子反应方程式为:CuO+2H+═Cu2++H2O,
故答案为:CuO+2H+═Cu2++H2O.
| ||
H2,
(1)由上述分析可知,A为CuO,B为Fe,C为CO2,D为Fe2O3,E为Cu,F为FeCl2,
故答案为:CuO;Fe;CO2;Fe2O3;Cu;FeCl2;
(2)反应①的离子反应方程式为:CuO+2H+═Cu2++H2O,
故答案为:CuO+2H+═Cu2++H2O.
点评:本题考查无机物推断,单质E为红色是推断突破口,再结合转化关系推断,注意掌握中学常见的化学工业,难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
下列事实可以证明氨水是弱碱的是( )
| A、0.1mol/L的氨水可以使酚酞试液变红 |
| B、0.1mol/L的氯化铵溶液的pH约为5 |
| C、氨水溶液的导电性比强碱溶液弱 |
| D、铵盐受热易分解 |

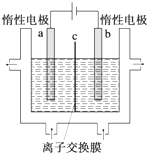 碘及其化合物在人类活动中占有重要地位.
碘及其化合物在人类活动中占有重要地位. 按要求完成下列问题
按要求完成下列问题