题目内容
解释下列有关实验现象:
(1)向氨水中滴几滴酚酞试液,溶液变红色: .
(2)两只棉球分别滴有几滴浓氨水和浓盐酸放入同一只烧杯中,用表面皿盖住烧杯口,烧杯内有白烟: .
(3)一瓶无色气体打开瓶盖后,瓶口呈现出红棕色: .
(4)切开的金属钠暴露在空气中,所发生反应的化学方程式是 .
(5)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是① 、② .
(1)向氨水中滴几滴酚酞试液,溶液变红色:
(2)两只棉球分别滴有几滴浓氨水和浓盐酸放入同一只烧杯中,用表面皿盖住烧杯口,烧杯内有白烟:
(3)一瓶无色气体打开瓶盖后,瓶口呈现出红棕色:
(4)切开的金属钠暴露在空气中,所发生反应的化学方程式是
(5)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是①
考点:氨的化学性质,钠的化学性质
专题:元素及其化合物
分析:(1)氨水溶液呈碱性;
(2)氨水、浓盐酸易挥发,二者反应生成氯化铵固体;
(3)瓶口呈现出红棕色,说明生成二氧化氮气体;
(4)钠不稳定,易与氧气反应;
(5)钠和水反应生成氢氧化钠和氢气,为放热反应,其的熔点较低.
(2)氨水、浓盐酸易挥发,二者反应生成氯化铵固体;
(3)瓶口呈现出红棕色,说明生成二氧化氮气体;
(4)钠不稳定,易与氧气反应;
(5)钠和水反应生成氢氧化钠和氢气,为放热反应,其的熔点较低.
解答:
解:(1)氨水中存在:NH3?H2O?OH-+NH4+,电离出OH-,溶液显碱性,遇酚酞试液变红色,
故答案为:氨水中的NH3?H2O电离出OH-,溶液显碱性,遇酚酞试液变红色;
(2)氨水、浓盐酸易挥发,二者反应生成氯化铵固体,形成白烟,
故答案为:浓氨水和浓盐酸挥发出的NH3 和HCl反应生成NH4Cl固体小颗粒,形成白烟;
(3)口呈现出红棕色,说明生成二氧化氮气体,瓶内含有无色的NO,故答案为:无色的NO气体挥发到空气中与O2反应生成红棕色的NO2;
(4)钠不稳定,易与氧气反应,反应的方程式为4Na+O2═2Na2O,故答案为:4Na+O2═2Na2O;
(5)钠和水反应生成氢氧化钠和氢气,为放热反应,其的熔点较低,故答案为:钠与水反应放出热量;钠的熔点低.
故答案为:氨水中的NH3?H2O电离出OH-,溶液显碱性,遇酚酞试液变红色;
(2)氨水、浓盐酸易挥发,二者反应生成氯化铵固体,形成白烟,
故答案为:浓氨水和浓盐酸挥发出的NH3 和HCl反应生成NH4Cl固体小颗粒,形成白烟;
(3)口呈现出红棕色,说明生成二氧化氮气体,瓶内含有无色的NO,故答案为:无色的NO气体挥发到空气中与O2反应生成红棕色的NO2;
(4)钠不稳定,易与氧气反应,反应的方程式为4Na+O2═2Na2O,故答案为:4Na+O2═2Na2O;
(5)钠和水反应生成氢氧化钠和氢气,为放热反应,其的熔点较低,故答案为:钠与水反应放出热量;钠的熔点低.
点评:本题综合考查元素化合物知识,为高考高频考点,侧重于基础知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
用NA代表阿伏加德罗常数,下列说法正确的是( )
| A、1molCl2作为氧化剂得到的电子数为NA |
| B、在标准状况下,11.2L水中含有分子数为0.5NA |
| C、0.3mol/LNa2SO4溶液中,所含Na+和SO42-总数为0.9NA |
| D、常温压下,64gSO2中含有的原子数为3NA |
当两个原子形成共价键时,原子的能量将( )
| A、都升高 |
| B、都降低 |
| C、都保持不变 |
| D、一个升高,一个降低 |
在碱性溶液中能大量共存且溶液为无色透明的离子组是( )
| A、Na+、Cu2+、Cl-、NO3- |
| B、Na+、NO3-、H+、CO32- |
| C、MnO4-、K+、HCO3- |
| D、K+、Na+、Cl-、NO3- |
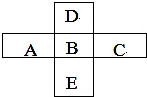 A、B、C、D、E五种主族元素所处周期表的位置如图所示.
A、B、C、D、E五种主族元素所处周期表的位置如图所示.

 表示的是(写粒子符号)
表示的是(写粒子符号)