题目内容
【题目】一定温度下,H2(g)与I2(g)反应生成HI(g),反应的能量变化如下图所示。下列说法不正确的是
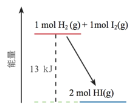
A.H2(g)+I2(g)=2HI(g) ΔH=-13kJ·mol1
B.反应物的总能量比生成物的总能量高
C.H2(g)和I2(g)的总能量比HI(g)的能量高13kJ
D.断裂反应物中化学键吸收的总能量比形成生成物中化学键放出的总能量低
【答案】C
【解析】
A.由图知反应是放热反应,△H=生成物所具有的能量总和-反应物所具有的能量总和=-13kJ·mol1,故A正确;
B.由纵坐标知,反应物的总能量比生成物的总能量高,故B正确;
C.由图知,1molH2(g)和1molI2(g)的总能量比2molHI(g)的能量高13kJ,故C错误;
D.由图知反应是放热反应,断裂反应物中化学键吸收的总能量比形成生成物中化学键放出的总能量低,故D正确;
故选C。

练习册系列答案
相关题目