题目内容
9.10mL某气态混合烃在80mL O2中充分燃烧,得到体积为65mL的混合气体(气体体积均在相同条件200C时测定),则该混合物不可能是( )| A. | 丙烷和丙烯 | B. | 乙烷和丙烯 | C. | 丙烯和丁炔 | D. | 丁烯和丙炔 |
分析 设混合烃的平均分子式为CxHy,烃充分燃烧的化学方程式为:CxHy+(x+$\frac{y}{4}$)O2$\frac{\underline{\;点燃\;}}{\;}$xCO2+$\frac{y}{2}$H2O(l),利用体积差量计算判断.
解答 解:设烃的分子式为CxHy,则:CxHy+(x+$\frac{y}{4}$)O2$\frac{\underline{\;点燃\;}}{\;}$xCO2+$\frac{y}{2}$H2O(l),体积减小
1 1+$\frac{y}{4}$
10mL 10mL+80mL-65mL=25mL
则1:(1+$\frac{y}{4}$)=10mL:25mL,
解得:y=6,
A.丙烷分子中含有8个H,丙烯分子中含有6个H,平均H原子数大于6,不可能为二者的混合物,故A正确;
B.乙烷分子中含有6个H,丙烯分子中含有6个H,二者的平均H原子一定为6,可以为二者的混合物,故B错误;
C.丙烯分子中含有6个H,丙炔分子中含有6个H,二者的平均H原子一定为6,可以为二者的混合物,故C错误;
D.丁烯分子中含有8个H,丙炔分子中含有4个H,二者的平均H原子数可以为6,可以是二者的混合物,故D错误;
故选A.
点评 本题混合物反应的计算,题目难度中等,侧重考查学生分析和解决问题的能力,注意利用燃烧通式进行解答,明确差量法的应用方法为解答关键,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
19.标准状况下,某同学向100mLH2S饱和溶液中通入SO2,所得溶液pH变化如图所示,下列分析中,正确的是( )
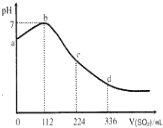

| A. | b 点对应的溶液导电性最强 | |
| B. | 亚硫酸是比氧硫酸更弱的酸 | |
| C. | 原H2S溶液的物质的量浓度为0.05mol•L-1 | |
| D. | ab段反应是:SO2+2H2S═3S↓+2H2O |
20.某气体在标准状况下的密度是1.25克/升,该气体的相对分子质量为( )
| A. | 26 | B. | 28 | C. | 30 | D. | 32 |
17.下列化学用语正确的是( )
| A. | 硅的原子结构示意图: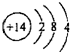 | |
| B. | 乙烯分子比例模型: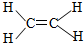 | |
| C. | 二氧化碳分子的电子式: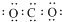 | |
| D. | 硫酸铁的电离方程式:Fe2(SO4)3═2Fe2++3SO42- |
14.下列有关离子方程错误的是( )
| A. | 将Fe加入CuSO4溶液中 Fe+Cu2+═Cu+Fe2+ | |
| B. | 向氯化铝溶液中加入足量氨水 Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ | |
| C. | 向Ca(OH)2溶液中通入过量 SO2SO2+OH-═HSO3- | |
| D. | 往水玻璃中加入盐酸 SiO32-+2H+═H2SiO3↓ |
1.下列物质属于酸的是( )
| A. | 二氧化硫 | B. | 生石灰 | C. | 三氧化硫 | D. | 硫酸 |
18.含有2~5个碳原子的直链烷烃沸点和燃烧热的数据见下表:
燃烧热:1mol物质完全燃烧,生成二氧化碳、液态水时所放出的热量.
根据表中数据,下列判断错误的是( )
| 烷烃名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 |
| 沸点/℃ | -88.6 | -42.1 | -0.5 | 36.1 |
| 燃烧热/KJ•mol-1 | 1559.8 | 2219.9 | 2877.6 | 3535.6 |
根据表中数据,下列判断错误的是( )
| A. | 正庚烷在常温常压下肯定不是气体 | |
| B. | 烷烃燃烧热和其所含碳原子数成线性关系 | |
| C. | 随碳原子数增加,烷烃沸点逐渐升高 | |
| D. | 随碳原子数增加,烷烃沸点和燃烧热都成比例增加 |
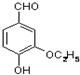 是食品添加剂的增香原料,其香味比香草醛更浓郁.
是食品添加剂的增香原料,其香味比香草醛更浓郁.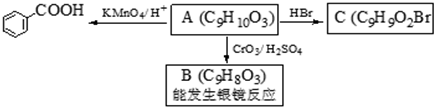
 .
. .
.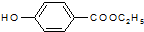 )是一种医药中间体,请设计合理方案用对甲基苯酚合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
)是一种医药中间体,请设计合理方案用对甲基苯酚合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).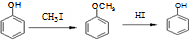
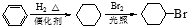
 .
.