题目内容
14.链式炔碳…-C≡C-C≡C-C≡C…是现已发现的碳的第四种同素异形体,已知链式炔碳C300经过适当的处理可得含多个-C≡C-(不含-C≡C-)的链状化合物C300H302,则该分子中含-C≡C-的数目为( )| A. | 73 | B. | 74 | C. | 75 | D. | 76 |
分析 对于烃CnHm,当分子中无C=C和环时,C≡C最多,当分子中有一个C≡C则氢原子与饱和烷烃相比减少4个氢原子,根据:叁键数=$\frac{(2n+2)-m}{4}$分析.
解答 解:对于烃CnHm,当分子中无C=C和环时,C≡C最多,当分子中有一个C≡C则氢原子与饱和烷烃相比减少4个氢原子,
叁键数=$\frac{2n+2-m}{4}=\frac{2×300+2-302}{4}$=75;故选C.
点评 本题考查有机化合物中碳的成键特征,难度较小,判断不饱和键时注意与饱和烷烃对比分析.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
4.关于元素周期表,下列叙述中不正确的是( )
| A. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| B. | 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 | |
| C. | 在金属元素区域可以寻找制备新型农药材料的元素 | |
| D. | 过渡元素是副族和第Ⅷ族元素的总称 |
5.根据如表推断下列说法中不正确的是( )
| 性质 | 金刚石 | 石墨 |
| 外观 | 无色,透明固体 | 灰黑,不透明固体 |
| 沸点 | ? | ? |
| 熔点 | ? | ? |
| 燃烧热/kJ•mol-1 | 395.4 | 393.5 |
| A. | C(石墨,s)═C(金刚石,s)△H=+1.9kJ•mol-1 | |
| B. | 在相同条件下石墨的熔点应高于金刚石 | |
| C. | 金刚石中碳碳键键能大于石墨中碳碳键键能 | |
| D. | 在相同条件下石墨和金刚石的沸点应相同 |
2.下列化学用语描述中不正确的是( )
| A. | 中子数为20的氯原子:${\;}_{17}^{37}Cl$ | |
| B. | K2O的电子式: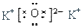 | |
| C. | HCO3-的电离方程式:HCO3-+H2O?CO32-+H3O+ | |
| D. | 比例模型 可以表示CO2分子或SiO2 可以表示CO2分子或SiO2 |
3.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4L CCl4含有的分子数为NA | |
| B. | 2.4gMg溶于足量稀盐酸,转移的电子数为0.1NA | |
| C. | 通常状况下,32gO2与32gO3所含的氧原子数均为2NA | |
| D. | 质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 的数目为NA |
4.设NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 3.4gNH3中含有电子数为2NA | |
| B. | 0.1mol/L CuSO4溶液中含有的SO2-4数目为0.1NA | |
| C. | 常温常压下,2.24L O3中含有的氧原子数为0.3NA | |
| D. | 8.7gMnO2与50mL 8mol/L浓盐酸充分反应后,生成Cl2的氯分子数为0.1NA |
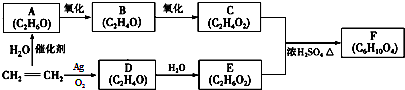
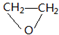 .
.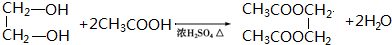 .
.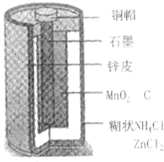 Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.
Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.